
বন্ধন কোণের কোন ক্রমটি সঠিক?
A.
H2O> NH3 > BeCl2 > BF3
B.
BF3>BeCl2>H2O>NH3
C.
BeCl2>NH3> BF3> H2O
D.
BeCl2>BF3>NH3>H2O
বন্ধন কোণের কোন ক্রমটি সঠিক?
সঠিক উত্তরঃ D.
BeCl2>BF3>NH3>H2O
Explanation:
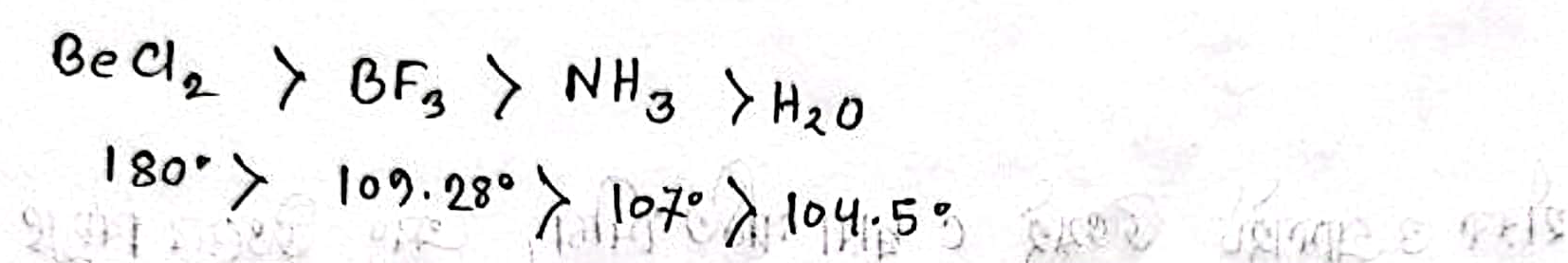
Another Explanation (5):
বন্ধন কোণ কোনো অণুর কেন্দ্রীয় পরমাণুর সাথে যুক্ত পরমাণুগুলোর মধ্যেকার কোণ। বিভিন্ন যৌগের বন্ধন কোণ বিভিন্ন হওয়ার কারণগুলো নিচে আলোচনা করা হলো:
প্রদত্ত ক্রম: BeCl2 > BF3 > NH3 > H2O
| যৌগ | কেন্দ্রীয় পরমাণু | মোট ইলেকট্রন জোড় | নিঃসঙ্গ জোড় | আকৃতি | আনুমানিক বন্ধন কোণ | ব্যাখ্যা |
|---|---|---|---|---|---|---|
| BeCl2 | Be | 2 | 0 | সরলরৈখিক (Linear) | 180° | বেরিলিয়ামের যোজ্যতা স্তরে ২টি ইলেকট্রন এবং কোনো নিঃসঙ্গ জোড় নেই। ফলে Cl-Be-Cl বন্ধন কোণ 180° হয়। |
| BF3 | B | 3 | 0 | সমতলীয় ত্রিভুজাকার (Trigonal Planar) | 120° | বোরণের যোজ্যতা স্তরে ৩টি ইলেকট্রন এবং কোনো নিঃসঙ্গ জোড় নেই। তাই F-B-F বন্ধন কোণ 120° হয়। |
| NH3 | N | 4 | 1 | পিরামিডীয় (Pyramidal) | 107° | নাইট্রোজেনের যোজ্যতা স্তরে ৪টি ইলেকট্রন জোড় (১টি নিঃসঙ্গ জোড়) থাকায় বন্ধন কোণ নিঃসঙ্গ জোড়ের বিকর্ষণের কারণে ১০৯.৫° থেকে কমে প্রায় ১০৭° হয়। 📉 |
| H2O | O | 4 | 2 | বাঁকানো (Bent) | 104.5° | অক্সিজেনের যোজ্যতা স্তরে ৪টি ইলেকট্রন জোড় (২টি নিঃসঙ্গ জোড়) থাকায় বন্ধন কোণ নিঃসঙ্গ জোড়ের বিকর্ষণের কারণে আরও কমে প্রায় ১০৪.৫° হয়। 💧 |
সুতরাং, নিঃসঙ্গ জোড়ের সংখ্যা বৃদ্ধির সাথে সাথে বন্ধন কোণ কমতে থাকে। এই কারণে BeCl2 > BF3 > NH3 > H2O ক্রমটি সঠিক। ✅