
A. bond pair-bond pair আকর্ষণ
B. bond pair-bond pair বিকর্ষণ
C. lond pair-lond pair বিকর্ষণ
D. কোনোটিই নয়
সঠিক উত্তরঃ C. lond pair-lond pair বিকর্ষণ
Explanation:
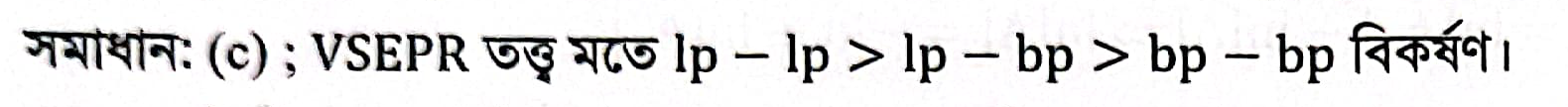
Another Explanation (5):
পানির (H2O) অণুতে বন্ধন কোণ ১০৯.৫° হওয়ার কথা থাকলেও বাস্তবে তা ১০৪° হয়। এর প্রধান কারণ হলো নিঃসঙ্গ ইলেকট্রন জোড় (lone pair) - নিঃসঙ্গ ইলেকট্রন জোড় বিকর্ষণ। নিচে বিস্তারিত আলোচনা করা হলো:
| বিকর্ষণের ধরন | শক্তির মাত্রা | প্রভাব |
|---|---|---|
| নিঃসঙ্গ জোড় - নিঃসঙ্গ জোড় | সবচেয়ে বেশি | বন্ধন কোণ সবচেয়ে বেশি কমায়। |
| নিঃসঙ্গ জোড় - বন্ধন জোড় | মাঝারি | বন্ধন কোণ কমায়। |
| বন্ধন জোড় - বন্ধন জোড় | সবচেয়ে কম | তুলনামূলকভাবে কম প্রভাব ফেলে। |
অক্সিজেনের নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণের কারণে পানির অণুর আকৃতি কৌণিক (bent) হয় এবং বন্ধন কোণ ১০৯.৫° এর পরিবর্তে ১০৪° হয়। এই বিকর্ষণ VSEPR (Valence Shell Electron Pair Repulsion) তত্ত্ব দ্বারা ব্যাখ্যা করা যায়।💡
আশা করি, পানির অণুতে বন্ধন কোণ কম হওয়ার কারণটি বোধগম্য হয়েছে।😊