Explanation:
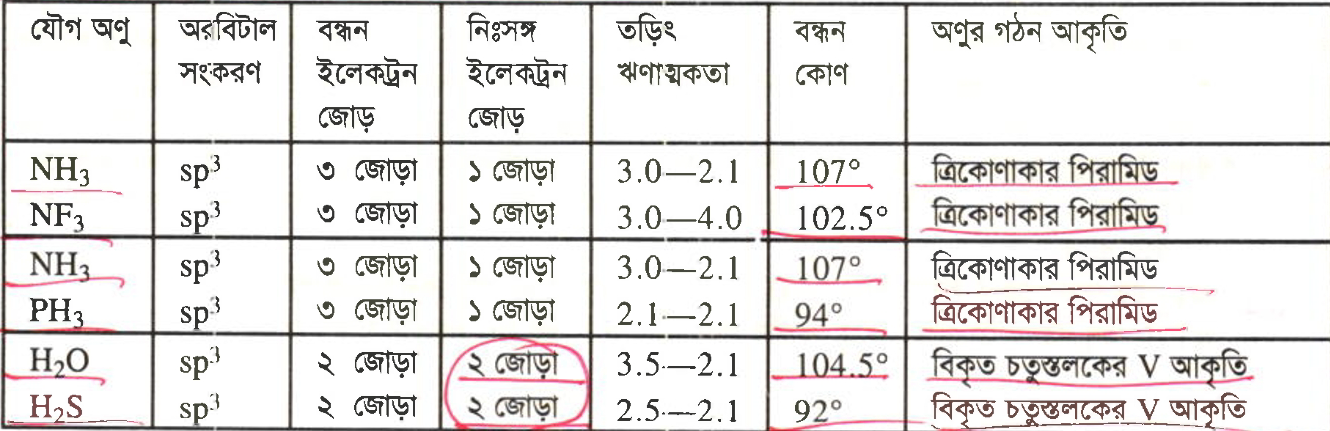
Another Explanation (5):
H2O অণুর আকৃতি 'V' হওয়ার কারণ
H2O (পানি) অণুর আকৃতি কৌণিক বা 'V' আকৃতির হওয়ার কারণ ব্যাখ্যা করা হলো:
কারণসমূহ
- অক্সিজেন পরমাণুর ইলেকট্রন বিন্যাস: অক্সিজেনের পারমাণবিক সংখ্যা ৮। এর ইলেকট্রন বিন্যাস 1s2 2s2 2p4। শেষ কক্ষপথে ৬টি ইলেকট্রন রয়েছে।
- দুটি O-H বন্ধন: অক্সিজেন পরমাণু দুটি হাইড্রোজেন পরমাণুর সাথে দুটি সমযোজী বন্ধন (covalent bond) গঠন করে। এই বন্ধনগুলো সরলরৈখিক হওয়ার কথা, কিন্তু...🤔
- অক্সিজেনে দুটি মুক্ত জোড় ইলেকট্রন: অক্সিজেনের শেষ কক্ষপথে দুটি নিঃসঙ্গ ইলেকট্রন জোড় (lone pair of electrons) বিদ্যমান। এই নিঃসঙ্গ ইলেকট্রন জোড়গুলো বন্ধন জোড় ইলেকট্রনগুলোর তুলনায় বেশি স্থান দখল করে। 😮
- বিকর্ষণ: নিঃসঙ্গ ইলেকট্রন জোড় এবং বন্ধন জোড় ইলেকট্রনগুলোর মধ্যে বিকর্ষণ ঘটে। নিঃসঙ্গ জোড় - নিঃসঙ্গ জোড় বিকর্ষণ, নিঃসঙ্গ জোড় - বন্ধন জোড় বিকর্ষণের চেয়ে শক্তিশালী। ফলে বন্ধন জোড়গুলো আরও কাছাকাছি চলে আসে। 😠😡
- VSEPR তত্ত্ব: ভ্যালেন্স শেল ইলেকট্রন পেয়ার রিপালসন (VSEPR) তত্ত্ব অনুসারে, ইলেকট্রন জোড়গুলো নিজেদের মধ্যে এমনভাবে বিকর্ষণ করে যাতে তারা নিউক্লিয়াসের চারপাশে সম্ভাব্য সবচেয়ে দূরে থাকতে পারে।
V আকৃতির গঠন
অক্সিজেনের নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণের কারণে H-O-H বন্ধন কোণ ১০৯.৫° থেকে কমে প্রায় ১০৪.৫° হয়। এর ফলে পানির অণুর আকৃতি 'V' আকৃতির হয়। 🎉
সারণী: ইলেকট্রন জোড় এবং বিকর্ষণ
| ইলেকট্রন জোড় |
বিকর্ষণ ক্ষমতা |
| নিঃসঙ্গ জোড় - নিঃসঙ্গ জোড় |
সবচেয়ে বেশি |
| নিঃসঙ্গ জোড় - বন্ধন জোড় |
মাঝারি |
| বন্ধন জোড় - বন্ধন জোড় |
সবচেয়ে কম |
ফলাফল
সুতরাং, H2O অণুর V আকৃতির হওয়ার প্রধান কারণ হলো অক্সিজেনের দুটি নিঃসঙ্গ ইলেকট্রন জোড়ের উপস্থিতি এবং তাদের বিকর্ষণ ক্ষমতা। 🥳
অতএব, সঠিক উত্তর: i ও ii

