
A. -13.6eV
B. -1.51eV
C. -2.72eV
D. -0.54eV
E. 0.54eV
সঠিক উত্তরঃ D. -0.54eV
Explanation:
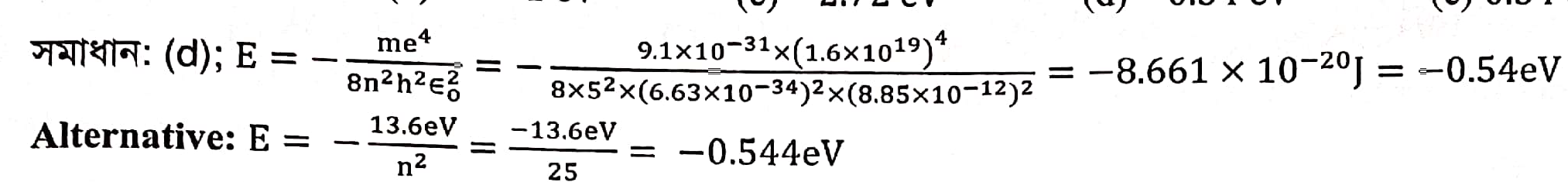
Another Explanation (5): ```html
আমরা জানি, হাইড্রোজেন পরমাণুর \(n\) তম বোর কক্ষের ইলেকট্রনের শক্তি:
\(E_n = -\frac{m e^4}{8 \epsilon_0^2 h^2 n^2}\) eV
এখানে,
এখন, মানগুলো বসালে পাই,
\(E_5 = -\frac{9.1 \times 10^{-31} \times (1.6 \times 10^{-19})^4}{8 \times (8.85 \times 10^{-12})^2 \times (6.626 \times 10^{-34})^2 \times 5^2}\) J
এই মানকে ইলেকট্রন ভোল্টে (eV) এ নিতে, \(1.6 \times 10^{-19}\) দিয়ে ভাগ করতে হবে:
\(E_5 = \frac{-\frac{9.1 \times 10^{-31} \times (1.6 \times 10^{-19})^4}{8 \times (8.85 \times 10^{-12})^2 \times (6.626 \times 10^{-34})^2 \times 5^2}}{1.6 \times 10^{-19}}\) eV
আমরা আরও সহজে \(E_n = \frac{-13.6}{n^2}\) eV এই সূত্র ব্যবহার করতে পারি। 😮
অতএব,
\(E_5 = \frac{-13.6}{5^2}\) eV
\(E_5 = \frac{-13.6}{25}\) eV
\(E_5 = -0.544\) eV
সুতরাং, হাইড্রোজেন পরমাণুর ৫ম বোর কক্ষের ইলেকট্রনের শক্তি প্রায় \(-0.54\) eV। 🎉
```