
A. 105
B. 109
C. 107
D. 120
সঠিক উত্তরঃ C. 107
Explanation:
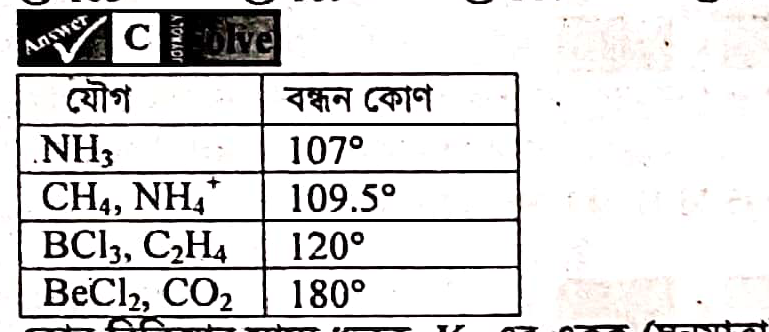
Another Explanation (5):
NH3 (অ্যামোনিয়া) অণুতে H-N-H বন্ধন কোণের মান 107°। 🤔 ব্যাখ্যা: অ্যামোনিয়া অণুর কেন্দ্রীয় পরমাণু নাইট্রোজেনের (N) চারটি ইলেকট্রন গ্রুপ রয়েছে: তিনটি বন্ধন জোড় (bonding pairs) 🤝 এবং একটি নিঃসঙ্গ জোড় (lone pair) 👤। এই চারটি ইলেকট্রন গ্রুপ চতুস্তলকীয়ভাবে (tetrahedrally) ⚶ সজ্জিত থাকতে চায়। কিন্তু নিঃসঙ্গ জোড় বন্ধন জোড়ের চেয়ে বেশি স্থান দখল করে, তাই এটি বন্ধন জোড়গুলোকে কিছুটা সংকুচিত করে। ফলে, আদর্শ চতুস্তলকীয় কোণ 109.5° থেকে H-N-H বন্ধন কোণ কমে 107° হয়। 📉 VSEPR (Valence Shell Electron Pair Repulsion) তত্ত্ব অনুসারে, ইলেকট্রন জোড়গুলো নিজেদের মধ্যে বিকর্ষণ করে এবং যতটা সম্ভব দূরে থাকতে চায়। নিঃসঙ্গ জোড়ের বিকর্ষণ বন্ধন জোড়ের বিকর্ষণের চেয়ে বেশি শক্তিশালী। 💪 \( \therefore \) NH3 অণুতে H-N-H বন্ধন কোণের মান = 107° 🤓