
নিচের কোন অনুতে বন্ধন কোন সর্বাধিক ?
A.
H2O
B.
BCI3
C.
NH3
D.
CH4
নিচের কোন অনুতে বন্ধন কোন সর্বাধিক ?
সঠিক উত্তরঃ B.
BCI3
Explanation:
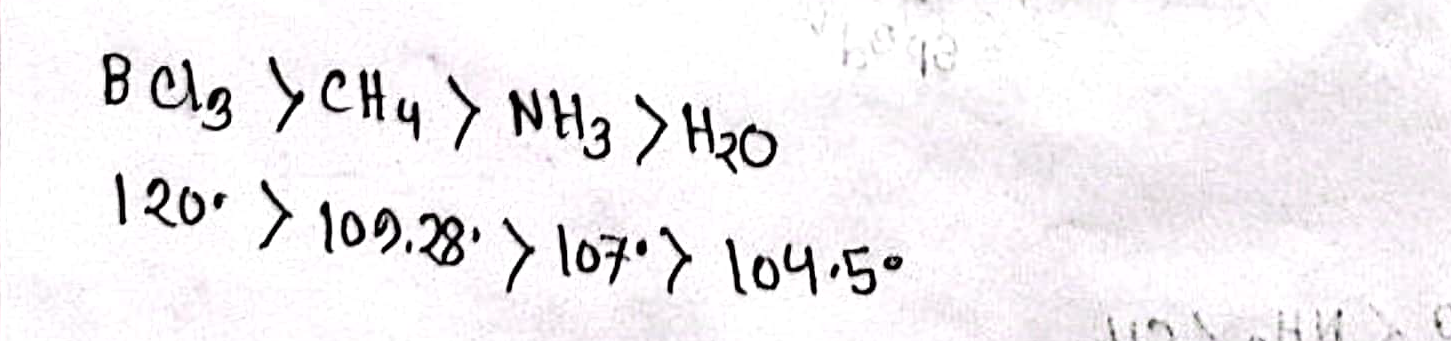
Another Explanation (5):
BCI3 (বোরন ট্রাইক্লোরাইড) যৌগের বন্ধন কোণ অন্যান্য যৌগগুলোর মধ্যে সর্বাধিক হওয়ার কারণ এর গঠন এবং পারিপার্শ্বিক বিষয়গুলোর উপর নির্ভরশীল। নিচে বিস্তারিত আলোচনা করা হলো:
বন্ধন কোণ হলো কোনো অণুতে দুটি বন্ধনের মধ্যে সৃষ্ট কোণ। এটি অণুর ত্রিমাত্রিক গঠন এবং আকৃতি নির্ধারণ করে। বন্ধন কোণ যত বেশি, অণু তত বেশি স্থিতিশীল হয়।⚛️
VSEPR তত্ত্ব অনুসারে, কোনো পরমাণুর যোজ্যতা স্তরের ইলেকট্রন জোড়গুলো (বন্ধন জোড় এবং নিঃসঙ্গ জোড়) একে অপরকে বিকর্ষণ করে এবং নিজেদের মধ্যে এমনভাবে অবস্থান নেয় যাতে বিকর্ষণ সর্বনিম্ন হয়। এর ফলে অণুর একটি নির্দিষ্ট জ্যামিতি তৈরি হয়।📐
BCI3 অণুতে বোরন পরমাণুর চারপাশে তিনটি বন্ধন জোড় রয়েছে এবং কোনো নিঃসঙ্গ জোড় নেই। তাই VSEPR তত্ত্ব অনুসারে, এর জ্যামিতি হলো ত্রিকোণীয় সমতলীয় (Trigonal Planar)। ত্রিকোণীয় সমতলীয় জ্যামিতিতে বন্ধন কোণ হয় 120°।✅
অন্যান্য অণুতে নিঃসঙ্গ জোড় অথবা বড় আকারের পরমাণু থাকলে বন্ধন কোণ BCI3-এর চেয়ে কম হতে পারে। যেমন: NH3 (অ্যামোনিয়া)-তে একটি নিঃসঙ্গ জোড় থাকার কারণে বন্ধন কোণ 107°।💧
| যৌগ | বন্ধন কোণ | কারণ |
|---|---|---|
| BCI3 | 120° | কোনো নিঃসঙ্গ জোড় নেই |
| NH3 | 107° | একটি নিঃসঙ্গ জোড় আছে |
| H2O | 104.5° | দুটি নিঃসঙ্গ জোড় আছে |
উপরের আলোচনা থেকে এটা স্পষ্ট যে, BCI3 যৌগে নিঃসঙ্গ ইলেকট্রন জোড় না থাকায় এবং ত্রিকোণীয় সমতলীয় জ্যামিতি বিদ্যমান থাকায় এর বন্ধন কোণ সর্বাধিক। 🎉