Explanation:
Another Explanation (5): ```html
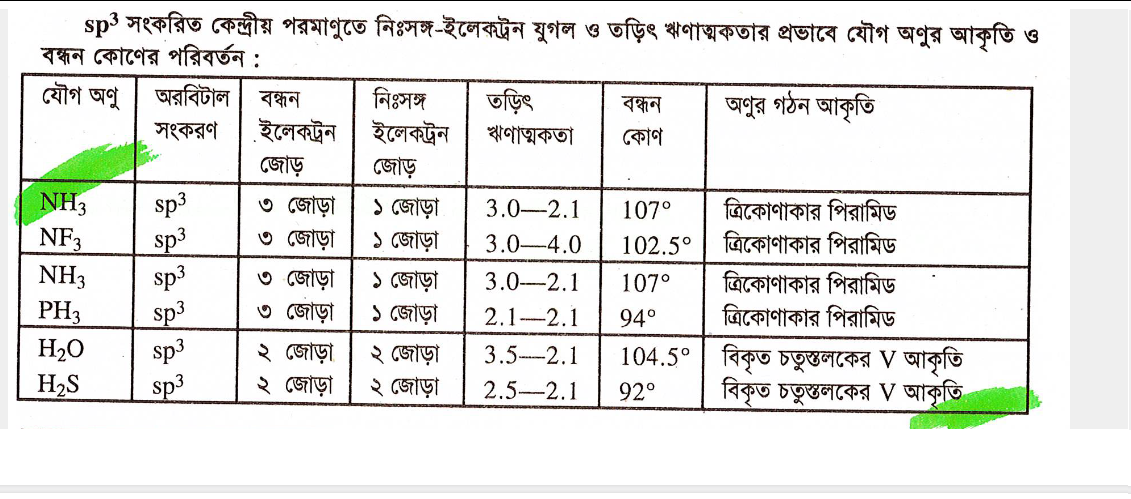
বন্ধন কোণ: H2O কেন ক্ষুদ্রতম? 💧
বন্ধন কোণ একটি গুরুত্বপূর্ণ বিষয় যা কোনো অণুর আকৃতি এবং বৈশিষ্ট্য নির্ধারণ করে। একাধিক যৌগের মধ্যে, পানির (H2O) বন্ধন কোণ তুলনামূলকভাবে ছোট। এর কারণগুলো নিচে আলোচনা করা হলো:
বন্ধন কোণ কী? 📐
বন্ধন কোণ হলো কোনো অণুতে দুটি বন্ধনের মধ্যে সৃষ্ট কোণ। এটি সাধারণত ডিগ্রিতে (°)-এ পরিমাপ করা হয়।
H2O-এর বন্ধন কোণ:
- H2O-এর বন্ধন কোণ প্রায় 104.5°।
- এটি চতুস্তলীয় (tetrahedral) জ্যামিতি থেকে সামান্য বিচ্যুত।
বন্ধন কোণ ছোট হওয়ার কারণসমূহ: 🤔
-
অক্সিজেনের নিঃসঙ্গ ইলেকট্রন জোড় (Lone Pair): অক্সিজেন পরমাণুর দুটি নিঃসঙ্গ ইলেকট্রন জোড় রয়েছে। এই নিঃসঙ্গ জোড়গুলো বন্ধন জোড়গুলোর (bonding pairs) উপর বিকর্ষণ বল প্রয়োগ করে।
👉 নিঃসঙ্গ জোড় - নিঃসঙ্গ জোড় বিকর্ষণ > নিঃসঙ্গ জোড় - বন্ধন জোড় বিকর্ষণ > বন্ধন জোড় - বন্ধন জোড় বিকর্ষণ
-
বিকর্ষণ বল (Repulsion): নিঃসঙ্গ ইলেকট্রন জোড়গুলোর মধ্যে বিকর্ষণ বন্ধন জোড়গুলোর মধ্যে বিকর্ষণের চেয়ে শক্তিশালী। এই কারণে, বন্ধন জোড়গুলো আরও কাছাকাছি চলে আসে, যার ফলে বন্ধন কোণ ছোট হয়ে যায়।
-
চতুস্তলীয় জ্যামিতি থেকে বিচ্যুতি: যদি নিঃসঙ্গ ইলেকট্রন জোড় না থাকতো, তবে H2O-এর বন্ধন কোণ চতুস্তলীয় জ্যামিতির কারণে 109.5° হতো। কিন্তু নিঃসঙ্গ জোড়ের বিকর্ষণের কারণে এটি কমে যায়।
তুলনামূলক আলোচনা: অন্যান্য যৌগের বন্ধন কোণ 📊
| যৌগ |
বন্ধন কোণ (প্রায়) |
কারণ |
| H2O |
104.5° |
দুটি নিঃসঙ্গ ইলেকট্রন জোড় |
| NH3 |
107° |
একটি নিঃসঙ্গ ইলেকট্রন জোড় |
| CH4 |
109.5° |
কোনো নিঃসঙ্গ ইলেকট্রন জোড় নেই |
উপসংহার 📝
H2O-এর ছোট বন্ধন কোণের প্রধান কারণ হলো অক্সিজেনের নিঃসঙ্গ ইলেকট্রন জোড়গুলোর বিকর্ষণ। এই বিকর্ষণের কারণে বন্ধন জোড়গুলো কাছাকাছি আসে এবং বন্ধন কোণ হ্রাস পায়। অন্যান্য যৌগের তুলনায়, H2O-এর গঠন এবং ইলেকট্রন বিন্যাস এটিকে বিশেষ করে তোলে। ⚛️
আশা করি, এই ব্যাখ্যাটি বোধগম্য হয়েছে। 😊
```

