Explanation:
Another Explanation (5):
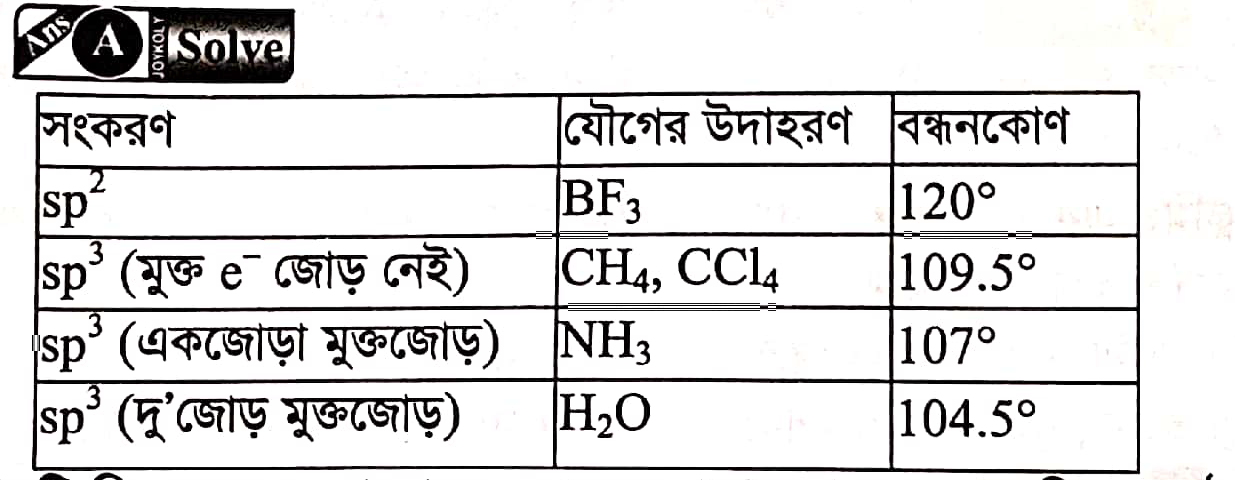
H2O এর বন্ধন কোণ: ১০৪.৫°
H2O (পানি) একটি কৌণিক আকৃতির অণু। এর বন্ধন কোণ ১০৪.৫° হওয়ার কারণ নিচে দেওয়া হলো:
- কেন্দ্রীয় পরমাণুর সংকরণ: পানির কেন্দ্রীয় পরমাণু অক্সিজেন (O)। অক্সিজেনের ইলেকট্রন বিন্যাস 1s2 2s2 2p4। এখানে অক্সিজেন sp3 সংক hybridised। ⚛️
- sp3 সংকরণের জ্যামিতি: sp3 সংকরণের কারণে চতুস্তলীয় (tetrahedral) জ্যামিতি হওয়ার কথা, যেখানে বন্ধন কোণ ১০৯.৫° হওয়ার কথা।📐
- লোন পেয়ারের বিকর্ষণ: অক্সিজেনের দুটি লোন পেয়ার ( নিঃসঙ্গ ইলেকট্রন জোড়) বিদ্যমান। লোন পেয়ার -লোন পেয়ার বিকর্ষণ, লোন পেয়ার-বন্ধন জোড় বিকর্ষণের চেয়ে বেশি শক্তিশালী। এই কারণে বন্ধন জোড়গুলো আরও কাছাকাছি চলে আসে। 😠➡️⬅️
- বিকর্ষণের প্রভাব: লোন পেয়ারগুলোর বিকর্ষণের কারণে স্বাভাবিক চতুস্তলীয় কোণ (১০৯.৫°) কিছুটা সংকুচিত হয়ে ১০৪.৫°-এ নেমে আসে। 📉
গাণিতিকভাবে ব্যাখ্যা করলে:
ধরা যাক, লোন পেয়ারের বিকর্ষণ \( \delta \) কোণে বন্ধন কোণ কমায়। তাহলে,
\( 109.5° - \delta = 104.5° \)
সুতরাং, পানির বন্ধন কোণ ১০৪.৫°, যা লোন পেয়ারের বিকর্ষণের কারণে সৃষ্ট। 🥰

