Explanation:
Another Explanation (5):
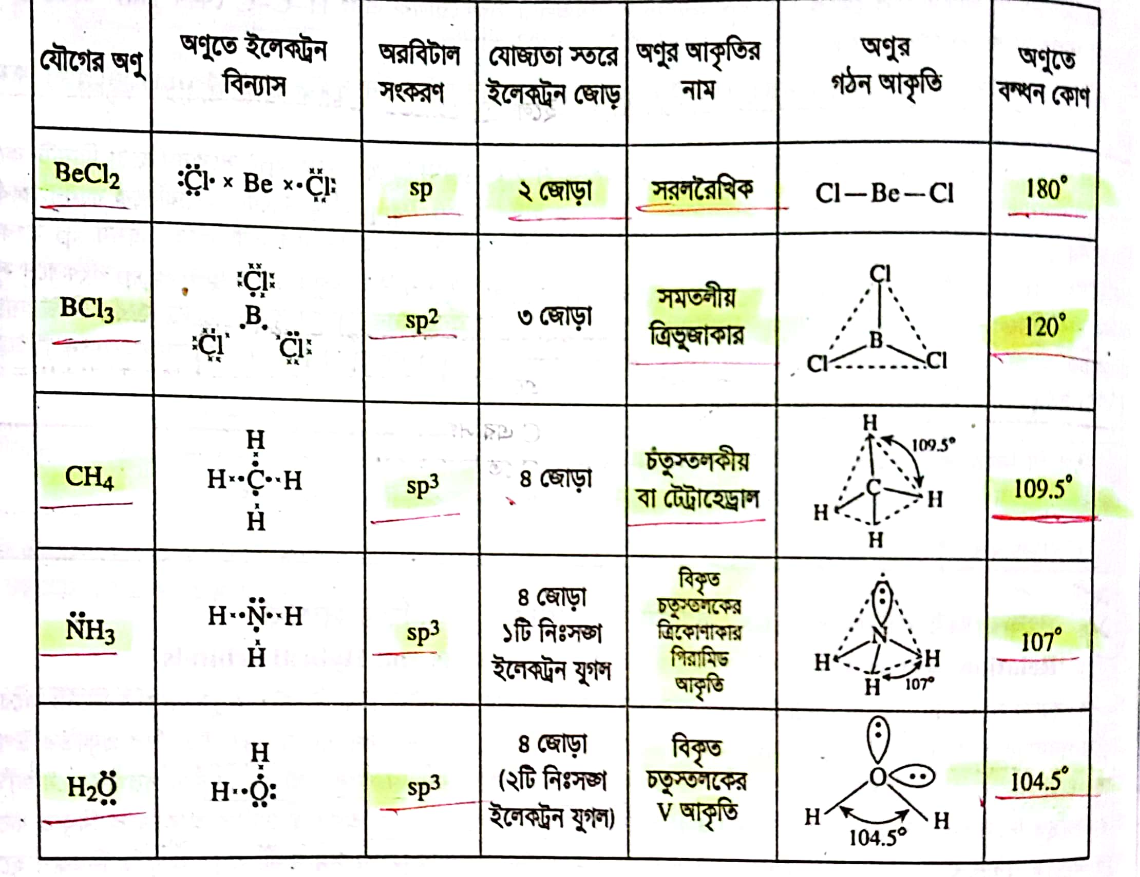
কোন যৌগটির বন্ধনকোণ ছোট: H2O এর ব্যাখ্যা 💧
H2O (পানি) যৌগের বন্ধনকোণ ছোট হওয়ার কারণ আলোচনা করা হলো:
বন্ধনকোণ ছোট হওয়ার কারণসমূহ 📝
-
কেন্দ্রীয় পরমাণুর নিঃসঙ্গ ইলেকট্রন জোড় 😒
-
অক্সিজেন (O) পরমাণুটি H2O যৌগের কেন্দ্রীয় পরমাণু।
-
অক্সিজেনের যোজ্যতা স্তরে ৬টি ইলেকট্রন থাকে। এর মধ্যে ২টি হাইড্রোজেন (H) পরমাণুর সাথে ২টি সমযোজী বন্ধন (covalent bond) তৈরি করে।
-
ফলে, অক্সিজেনের উপর ২টি নিঃসঙ্গ ইলেকট্রন জোড় (lone pair of electrons) থাকে। এই নিঃসঙ্গ ইলেকট্রন জোড় বন্ধন ইলেকট্রন জোড়কে বিকর্ষণ করে।
নিঃসঙ্গ ইলেকট্রন জোড় > বন্ধন ইলেকট্রন জোড় এর বিকর্ষণ
- এই বিকর্ষণের কারণে বন্ধনকোণ স্বাভাবিকের চেয়ে কমে যায়।
-
VSEPR তত্ত্ব (Valence Shell Electron Pair Repulsion Theory) 🤓
- VSEPR তত্ত্ব অনুযায়ী, ইলেকট্রন জোড়গুলো (বন্ধন এবং নিঃসঙ্গ) নিজেদের মধ্যে এমনভাবে বিকর্ষণ করে যাতে তারা কেন্দ্রীয় পরমাণুর চারপাশে সম্ভাব্য সর্বোচ্চ দূরত্বে অবস্থান করতে পারে।
- H2O যৌগে অক্সিজেনের চারপাশে ৪টি ইলেকট্রন জোড় (২টি বন্ধন জোড় এবং ২টি নিঃসঙ্গ জোড়) থাকায় এরা চতুস্তলকীয়ভাবে (tetrahedrally) থাকার চেষ্টা করে।
- কিন্তু নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ বেশি হওয়ার কারণে চতুস্তলকীয় কোণ (109.5°) থেকে বন্ধনকোণ কমে যায়।
-
হাইড্রোজেনের ছোট আকার 👶
- হাইড্রোজেন পরমাণুগুলোর আকার ছোট হওয়ায় এদের মধ্যে বিকর্ষণ কম থাকে।
- ফলে, নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণই প্রধান হয়ে দাঁড়ায় এবং বন্ধনকোণ সংকুচিত হয়।
H2O এর বন্ধনকোণ 📐
H2O যৌগের বন্ধনকোণ প্রায় 104.5°।
তুলনামূলক আলোচনা 📊
| যৌগ |
বন্ধনকোণ (°) |
কারণ |
| H2O |
104.5 |
দুটি নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ 😒 |
| NH3 (অ্যামোনিয়া) |
107 |
একটি নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ 🙄 |
| CH4 (মিথেন) |
109.5 |
কোনো নিঃসঙ্গ ইলেকট্রন জোড় নেই 😊 |
উপরের তুলনা থেকে স্পষ্ট যে, নিঃসঙ্গ ইলেকট্রন জোড়ের সংখ্যা বাড়লে বন্ধনকোণ ছোট হয়ে যায়। 👍
সারসংক্ষেপ 💡
H2O যৌগের বন্ধনকোণ ছোট হওয়ার মূল কারণ হলো অক্সিজেনের উপর দুটি নিঃসঙ্গ ইলেকট্রন জোড়ের উপস্থিতি। এই নিঃসঙ্গ ইলেকট্রন জোড়গুলো বন্ধন ইলেকট্রন জোড়কে প্রবলভাবে বিকর্ষণ করে, যার ফলে বন্ধনকোণ সংকুচিত হয়ে 104.5° তে নেমে আসে।

