
কোন যৌগটিতে বন্ধন কোণ সর্বোচ্চ?
A.
C2H2
B.
C2H4
C.
NH3
D.
H2S
কোন যৌগটিতে বন্ধন কোণ সর্বোচ্চ?
সঠিক উত্তরঃ A.
C2H2
Explanation:
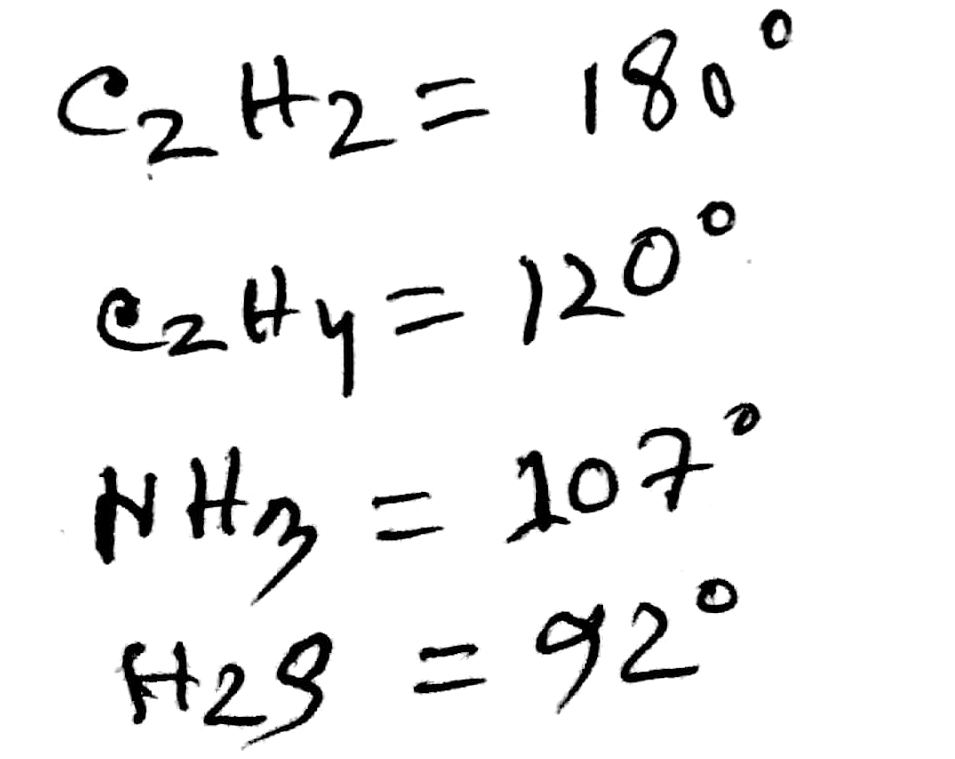
Another Explanation (5):
উত্তর: C2H2
কোন যৌগের বন্ধন কোণ নির্ভর করে মূলত কেন্দ্রীয় পরমাণুর সংকরণ (Hybridization) এবং তার চারপাশে থাকা lone pair ইলেকট্রনের উপর। নিচে কয়েকটি যৌগের বন্ধন কোণ এবং তাদের কারণ আলোচনা করা হলো:
| যৌগ | সংকরায়ণ | বন্ধন কোণ (প্রায়) | আকৃতি | কারণ |
|---|---|---|---|---|
| CH4 (মিথেন) 🏠 | sp3 | 109.5° | চতুস্তলকীয় (Tetrahedral) | sp3 সংকরায়ণের কারণে চারটি সিগমা বন্ধন গঠিত হয়। |
| NH3 (অ্যামোনিয়া) 💨 | sp3 | 107° | পিরামিডীয় (Pyramidal) | sp3 সংকরায়ণ হলেও একটি lone pair থাকায় বন্ধন কোণ কমে যায়। |
| H2O (পানি) 💧 | sp3 | 104.5° | V-আকৃতির (Bent) | sp3 সংকরায়ণ এবং দুটি lone pair এর বিকর্ষণের কারণে বন্ধন কোণ আরও কমে যায়। |
| BF3 (বোরন ট্রাইফ্লুরাইড) | sp2 | 120° | ত্রিকোণীয় সমতলীয় (Trigonal Planar) | sp2 সংকরায়ণের কারণে তিনটি সিগমা বন্ধন গঠিত হয়। |
লক্ষ্যনীয়: lone pair ইলেকট্রন বন্ধন কোণ কমিয়ে দেয়। যত বেশি lone pair, বন্ধন কোণ তত কম। 📉
অতএব, C2H2 যৌগে বন্ধন কোণ সর্বোচ্চ (180°), কারণ এর কার্বন পরমাণু sp সংকরিত এবং এতে কোনো lone pair নেই। 🎉
আশা করি, ব্যাখ্যাটি বোধগম্য হয়েছে! 😊