Explanation:
Another Explanation (5):
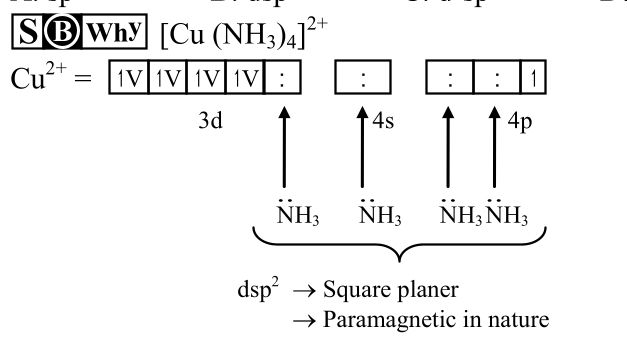
[Cu(NH3)4]2+ আয়নে কপারের সংকরণ: dsp2
Cu(II) জটিল আয়ন [Cu(NH3)4]2+ এ কপারের সংকরণ dsp2 হওয়ার কারণ নিচে ব্যাখ্যা করা হলো:
ব্যাখ্যা:
- কপারের ইলেকট্রন বিন্যাস: কপার (Cu) এর ইলেকট্রন বিন্যাস হলো [Ar] 3d104s1। Cu2+ আয়ন তৈরি হওয়ার সময় দুটি ইলেকট্রন অপসারিত হয়। ফলে Cu2+ আয়নের ইলেকট্রন বিন্যাস দাঁড়ায় [Ar] 3d9।
- লিগ্যান্ডের সাথে বন্ধন গঠন: [Cu(NH3)4]2+ জটিল আয়নে কপার চারটি অ্যামোনিয়া (NH3) লিগ্যান্ডের সাথে সন্নিবেশ বন্ধন (coordinate bond) তৈরি করে। অ্যামোনিয়া একটি শক্তিশালী লিগ্যান্ড।
- ইলেকট্রনের পুনর্বিন্যাস ও সংকরণ: শক্তিশালী লিগ্যান্ডের প্রভাবে Cu2+ আয়নের 3d ইলেকট্রনগুলো পুনর্বিন্যাসিত হয়। একটি 4s এবং দুটি 4p অরবিটাল ও একটি 3d অরবিটাল মিশ্রিত হয়ে চারটি নতুন dsp2 সংকর অরবিটাল তৈরি করে।
- সন্নিবেশ বন্ধন গঠন: প্রতিটি NH3 লিগ্যান্ড তার lone pair ইলেকট্রন দিয়ে কপারের dsp2 সংকর অরবিটালে সন্নিবেশ বন্ধন তৈরি করে। এর ফলে চারটি Cu-N বন্ধন গঠিত হয়।
- জ্যামিতি: dsp2 সংকরণের কারণে জটিল আয়নটির জ্যামিতি হয় বর্গাকার সমতলীয় (square planar)।

বর্গাকার সমতলীয় জ্যামিতি
সংক্ষেপে:
- Cu2+ আয়ন: [Ar] 3d9
- লিগ্যান্ড: 4টি NH3 (শক্তিশালী লিগ্যান্ড)
- সংকরায়ন: dsp2
- জ্যামিতি: বর্গাকার সমতলীয়
টেবিলের মাধ্যমে উপস্থাপন:
| বৈশিষ্ট্য |
মান |
| কেন্দ্রীয় আয়ন |
Cu2+ |
| ইলেকট্রন বিন্যাস |
[Ar] 3d9 |
| লিগ্যান্ড |
4 NH3 |
| সংকরায়ন |
dsp2 |
| জ্যামিতি |
বর্গাকার সমতলীয় |
সুতরাং, [Cu(NH3)4]2+ আয়নে কপারের dsp2 সংকরণ ঘটে। ✅
আশা করি, এটি আপনার বুঝতে সাহায্য করবে। 😊


