
বন্ধন কোণ বৃদ্ধির সঠিক ক্রম কোনটি?
A.
NH3 < CH4 < H2S < H2O
B.
H₂S < H2O < NH3 < CH4
C.
NH3 < H2O < CH4 < H₂S
D.
CH4 < H₂S < H2O < NH3
বন্ধন কোণ বৃদ্ধির সঠিক ক্রম কোনটি?
সঠিক উত্তরঃ B.
H₂S < H2O < NH3 < CH4
Explanation:
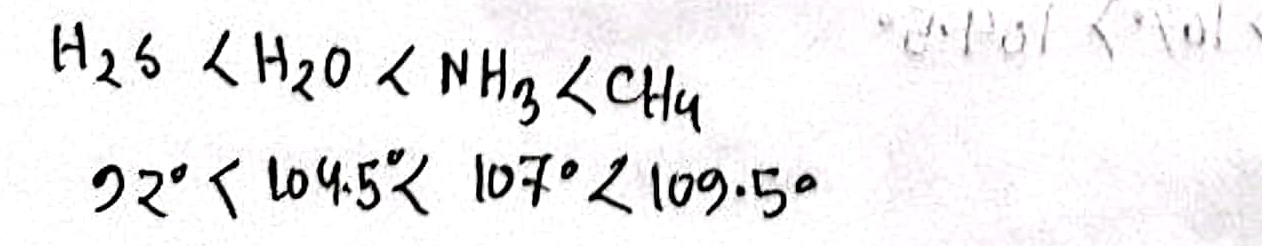
Another Explanation (5):
বন্ধন কোণ (Bond angle) হলো কোনো অণুতে (Molecule) দুটি বন্ধনের (Bond) মধ্যেকার কোণ। কেন্দ্রীয় পরমাণুর (Central atom) সঙ্গে যুক্ত পরমাণুগুলোর অবস্থানের উপর এটি নির্ভর করে। বিভিন্ন কারণে বন্ধন কোণের পরিবর্তন হতে পারে, যার মধ্যে উল্লেখযোগ্য হলো:
আলোচ্য যৌগগুলোর বন্ধন কোণের সঠিক ক্রম হলো: H₂S < H₂O < NH₃ < CH₄। নিচে কারণগুলো ব্যাখ্যা করা হলো:
সালফার (S) কেন্দ্রীয় পরমাণু। অক্সিজেনের (O) তুলনায় সালফারের আকার বড় হওয়ায় এবং তড়িৎ ঋণাত্মকতা কম হওয়ায় বন্ধন জোড় ইলেকট্রনগুলো (Bond pair electrons) কেন্দ্র থেকে দূরে থাকে। ফলে বিকর্ষণ কম হয় এবং বন্ধন কোণ ছোট হয়। H₂S এর বন্ধন কোণ প্রায় 92° 📉।
অক্সিজেন (O) কেন্দ্রীয় পরমাণু। অক্সিজেনের দুটি নিঃসঙ্গ ইলেকট্রন জোড় (lone pair) থাকায় বন্ধন জোড়গুলোর মধ্যে বিকর্ষণ ঘটে। নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ বন্ধন জোড়ের বিকর্ষণের চেয়ে বেশি শক্তিশালী হওয়ায় বন্ধন কোণ স্বাভাবিকের চেয়ে কম হয়। H₂O এর বন্ধন কোণ প্রায় 104.5° 💧।
নাইট্রোজেন (N) কেন্দ্রীয় পরমাণু। অ্যামোনিয়াতে একটি নিঃসঙ্গ ইলেকট্রন জোড় বিদ্যমান। নিঃসঙ্গ ইলেকট্রন জোড়ের কারণে বন্ধন জোড়গুলো সামান্য সংকুচিত হয়, ফলে চতুস্তলকীয় কোণ (Tetrahedral angle) 109.5° থেকে কমে যায়। NH₃ এর বন্ধন কোণ প্রায় 107° 🌬️।
কার্বন (C) কেন্দ্রীয় পরমাণু। মিথেনে কোনো নিঃসঙ্গ ইলেকট্রন জোড় নেই। কার্বনের চারটি হাত চারটি হাইড্রোজেন পরমাণুর সাথে সমভাবে যুক্ত থাকায় এদের মধ্যে বিকর্ষণ সর্বনিম্ন হয় এবং এটি একটি সুষম চতুস্তলকীয় গঠন (Regular tetrahedral) তৈরি করে। CH₄ এর বন্ধন কোণ 109.5° 🌡️।
| যৌগ (Compound) | কেন্দ্রীয় পরমাণু (Central Atom) | নিঃসঙ্গ ইলেকট্রন জোড় (Lone Pair) | বন্ধন কোণ (Bond Angle) | বৈশিষ্ট্য (Features) |
|---|---|---|---|---|
| H₂S | S | ২ টি | প্রায় 92° | S এর আকার বড় ও তড়িৎ ঋণাত্মকতা কম 😥 |
| H₂O | O | ২ টি | প্রায় 104.5° | নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ বেশি 😒 |
| NH₃ | N | ১ টি | প্রায় 107° | নিঃসঙ্গ ইলেকট্রন জোড়ের প্রভাবে সংকুচিত 😟 |
| CH₄ | C | ০ টি | 109.5° | সুষম চতুস্তলকীয় গঠন 😊 |
সুতরাং, নিঃসঙ্গ ইলেকট্রন জোড়ের সংখ্যা এবং কেন্দ্রীয় পরমাণুর আকারের উপর ভিত্তি করে বন্ধন কোণের ক্রম নির্ধারিত হয়।
আশা করি, এই ব্যাখ্যাটি বন্ধন কোণ সম্পর্কে আপনার ধারণা স্পষ্ট করতে সাহায্য করবে। 👍