
কোনটির বন্ধন কোণ সবচেয়ে কম ?
A.
BeCl2
B.
BCI3
C.
CH4
D.
NH3
কোনটির বন্ধন কোণ সবচেয়ে কম ?
সঠিক উত্তরঃ D.
NH3
Explanation:
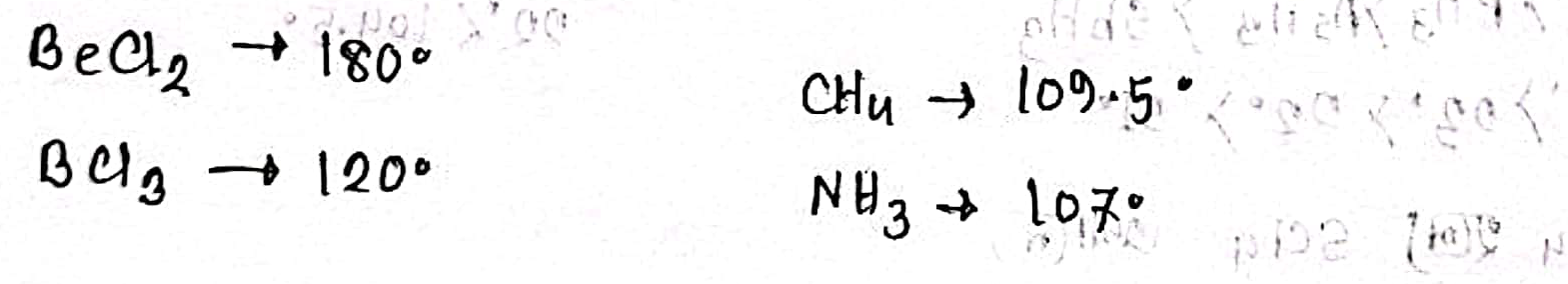
Another Explanation (5):
এখানে NH3 এর বন্ধন কোণ কেন সবচেয়ে কম, তা ব্যাখ্যা করা হলো:
কোনো যৌগের বন্ধন কোণ মূলত ঐ যৌগের কেন্দ্রীয় পরমাণুর চারপাশে থাকা পরমাণু এবং নিঃসঙ্গ জোড় ইলেকট্রন (lone pair electron) এর বিন্যাসের উপর নির্ভর করে। VSEPR (Valence Shell Electron Pair Repulsion) তত্ত্ব অনুসারে, ইলেকট্রনগুলো নিজেদের মধ্যে বিকর্ষণ করে এবং যতটা সম্ভব দূরে থাকতে চায়। নিঃসঙ্গ জোড় ইলেকট্রন, বন্ধন জোড় ইলেকট্রনের চেয়ে বেশি বিকর্ষণ করে।
অ্যামোনিয়াতে নাইট্রোজেন পরমাণুর সাথে তিনটি হাইড্রোজেন পরমাণু যুক্ত থাকে এবং একটি নিঃসঙ্গ জোড় ইলেকট্রন থাকে। এই নিঃসঙ্গ জোড় ইলেকট্রন বন্ধন জোড় ইলেকট্রনগুলোর উপর অতিরিক্ত বিকর্ষণ বল প্রয়োগ করে।
| যৌগ | বন্ধন কোণ | কারণ |
|---|---|---|
| CH4 (মিথেন) | 109.5° | কোনো নিঃসঙ্গ জোড় ইলেকট্রন নেই 😊। সুষম চতুস্তলীয় গঠন। |
| NH3 (অ্যামোনিয়া) | 107° | একটি নিঃসঙ্গ জোড় ইলেকট্রন বন্ধন জোড়গুলোকে বিকর্ষণ করে। তাই চতুস্তলীয় গঠন সামান্য সংকুচিত হয়। 😥 |
| H2O (পানি) | 104.5° | দুটি নিঃসঙ্গ জোড় ইলেকট্রন বন্ধন জোড়গুলোকে আরও বেশি বিকর্ষণ করে। ফলে বন্ধন কোণ আরও কমে যায়। 😫 |
অ্যামোনিয়া (NH3) যৌগে একটি নিঃসঙ্গ জোড় ইলেকট্রন থাকায় এর বন্ধন কোণ মিথেন (CH4) এর চেয়ে কম। নিঃসঙ্গ জোড় ইলেকট্রনের বিকর্ষণ বলের কারণেই এমনটা হয়। 🥳