Explanation:
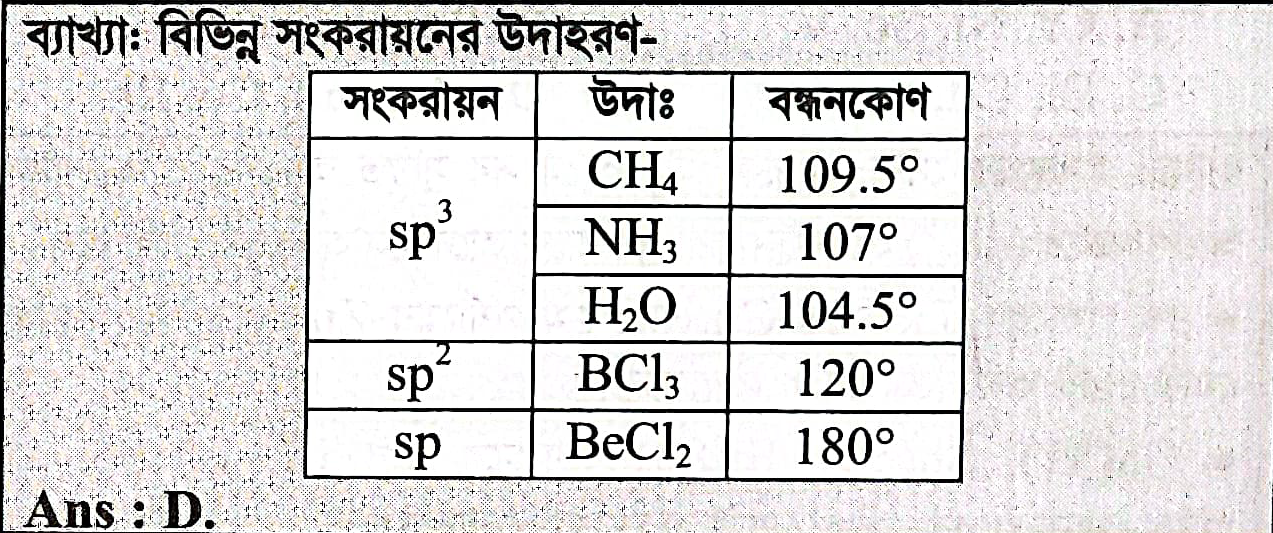
Another Explanation (5):
BCl3 যৌগে বন্ধন কোণের মান সর্বাধিক কেন? 🧐
BCl3 যৌগে বন্ধন কোণের মান অন্যান্য যৌগ থেকে বেশি হওয়ার প্রধান কারণগুলো নিচে আলোচনা করা হলো:
কারণসমূহ:
- কেন্দ্রীয় পরমাণুর জ্যামিতি: BCl3 যৌগের কেন্দ্রীয় পরমাণু হলো বোরন (B)। বোরনের তিনটি যোজ্যতা ইলেকট্রন আছে যা তিনটি ক্লোরিন (Cl) পরমাণুর সাথে সমযোজী বন্ধন তৈরি করে। এই তিনটি বন্ধন ইলেকট্রন মেঘ ত্রিমাত্রিকভাবে এমনভাবে বিন্যস্ত থাকে যাতে তারা একে অপরের থেকে দূরে থাকতে পারে। ফলে এর জ্যামিতি ত্রিকোণাকার সমতলীয় (Trigonal Planar) হয়। 📐
- বিকর্ষণ সর্বনিম্নকরণ: ত্রিকোণাকার সমতলীয় জ্যামিতিতে তিনটি বন্ধন ইলেকট্রন মেঘের মধ্যে বিকর্ষণ সর্বনিম্ন হয়। যেহেতু তিনটি বন্ধনই সমানভাবে বিন্যস্ত থাকে, তাই প্রতিটি বন্ধনের মধ্যে কোণ হয় 120°। 👌
- নিঃসঙ্গ জোড় ইলেকট্রনের অনুপস্থিতি: বোরনের কোনো নিঃসঙ্গ জোড় (Lone pair) ইলেকট্রন নেই। নিঃসঙ্গ জোড় ইলেকট্রন বন্ধন জোড় ইলেকট্রনের চেয়ে বেশি বিকর্ষণ করে, যার ফলে বন্ধন কোণের মান কমে যেতে পারে। BCl3 যৌগে নিঃসঙ্গ জোড় ইলেকট্রন না থাকায় বন্ধন কোণ 120° থাকে। 👍
- VSEPR তত্ত্ব: ভ্যালেন্স শেল ইলেকট্রন পেয়ার রিপালশন (VSEPR) তত্ত্ব অনুসারে, ইলেকট্রন মেঘগুলো এমনভাবে নিজেদেরকে সাজিয়ে নেয় যাতে বিকর্ষণ সর্বনিম্ন হয়। BCl3 যৌগের ক্ষেত্রে, ত্রিকোণাকার সমতলীয় জ্যামিতি এই শর্তটি পূরণ করে।
তুলনামূলক আলোচনা:
অন্যান্য যৌগ যেমন অ্যামোনিয়া (NH3) বা জল (H2O) এর ক্ষেত্রে নিঃসঙ্গ জোড় ইলেকট্রন থাকায় বন্ধন কোণের মান কমে যায়। 👇
| যৌগ |
জ্যামিতি |
বন্ধন কোণ |
নিঃসঙ্গ জোড় ইলেকট্রন |
| BCl3 |
ত্রিকোণাকার সমতলীয় |
120° |
নেই |
| NH3 |
ত্রিকোণাকার পিরামিডীয় |
107° |
আছে (১টি) |
| H2O |
কৌণিক |
104.5° |
আছে (২টি) |
সংক্ষেপে:
BCl3 যৌগের ত্রিকোণাকার সমতলীয় জ্যামিতি এবং নিঃসঙ্গ জোড় ইলেকট্রনের অনুপস্থিতির কারণে বন্ধন কোণের মান সবচেয়ে বেশি (120°)। 🎉
আশা করি, ব্যাখ্যাটি আপনার বোধগম্য হয়েছে। 😊

