Explanation:
Another Explanation (5):
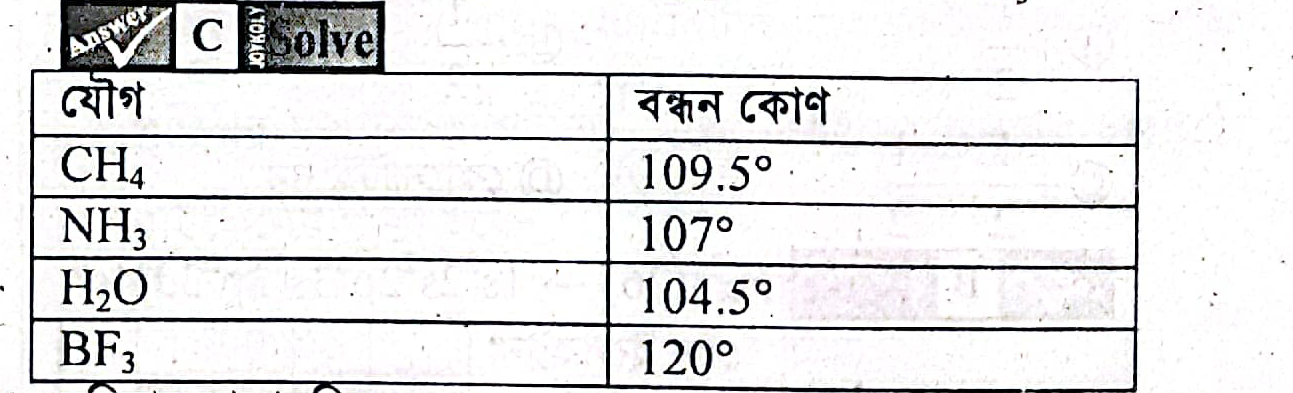
H2O এর বন্ধন কোণ সবচেয়ে কম কেন? 🤔
H2O (পানি) যৌগের বন্ধন কোণ অন্যান্য যৌগগুলোর মধ্যে সাধারণত সর্বনিম্ন হয়ে থাকে। এর কারণগুলো নিচে আলোচনা করা হলো:
কারণসমূহ:
-
কেন্দ্রীয় পরমাণুর নিঃসঙ্গ ইলেকট্রন জোড় (Lone Pair): অক্সিজেন (O) পরমাণুর দুটি নিঃসঙ্গ ইলেকট্রন জোড় রয়েছে। এই নিঃসঙ্গ ইলেকট্রন জোড়গুলো বন্ধন জোড়গুলোর (Bond Pair) উপর বিকর্ষণ বল প্রয়োগ করে। 😒
-
VSEPR তত্ত্ব (Valence Shell Electron Pair Repulsion Theory): VSEPR তত্ত্ব অনুযায়ী, ইলেকট্রন জোড়গুলো (বন্ধন জোড় ও নিঃসঙ্গ জোড়) নিজেদের মধ্যে এমনভাবে বিকর্ষণ করে যাতে তারা কেন্দ্রীয় পরমাণুর চারপাশে যতটা সম্ভব দূরে থাকতে পারে। নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ ক্ষমতা বন্ধন জোড়ের চেয়ে বেশি। 😠
-
বিকর্ষণের ক্রম: নিঃসঙ্গ জোড়-নিঃসঙ্গ জোড় > নিঃসঙ্গ জোড়-বন্ধন জোড় > বন্ধন জোড়-বন্ধন জোড়। অর্থাৎ, দুটি নিঃসঙ্গ ইলেকট্রন জোড়ের মধ্যে বিকর্ষণ সবচেয়ে বেশি, এরপর একটি নিঃসঙ্গ ও একটি বন্ধন জোড়ের মধ্যে এবং সবশেষে দুটি বন্ধন জোড়ের মধ্যে বিকর্ষণ সবচেয়ে কম। এই কারণে পানির বন্ধন কোণ সামান্য সংকুচিত হয়ে যায়।
তুলনামূলক আলোচনা (সারণী):
| যৌগ |
বন্ধন কোণ (প্রায়) |
কারণ |
| H2O |
104.5° |
দুটি নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ |
| NH3 |
107° |
একটি নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ |
| CH4 |
109.5° |
কোনো নিঃসঙ্গ ইলেকট্রন জোড় নেই |
উপরের সারণী থেকে দেখা যায়, মিথেন (CH4) এ কোনো নিঃসঙ্গ ইলেকট্রন জোড় না থাকায় এর বন্ধন কোণ স্বাভাবিক চতুস্তলীয় (tetrahedral) কোণ (109.5°)। অ্যামোনিয়া (NH3) তে একটি নিঃসঙ্গ ইলেকট্রন জোড় থাকায় এর বন্ধন কোণ সামান্য কমে যায় (107°)। কিন্তু পানিতে (H2O) দুটি নিঃসঙ্গ ইলেকট্রন জোড় থাকায় বিকর্ষণ সবচেয়ে বেশি হয় এবং বন্ধন কোণ আরও কমে 104.5° তে পৌঁছায়। 🥰
সংক্ষেপে:
- অক্সিজেনের দুটি নিঃসঙ্গ জোড় আছে।
- নিঃসঙ্গ জোড় বন্ধন জোড়কে বিকর্ষণ করে।
- VSEPR তত্ত্ব অনুযায়ী নিঃসঙ্গ জোড়ের বিকর্ষণ বেশি।
- তাই H2O এর বন্ধন কোণ সর্বনিম্ন।🥳
আশা করি, H2O এর বন্ধন কোণ কেন সবচেয়ে কম, তা এখন স্পষ্ট হয়েছে। 😊

