Explanation:
Another Explanation (5): ```html
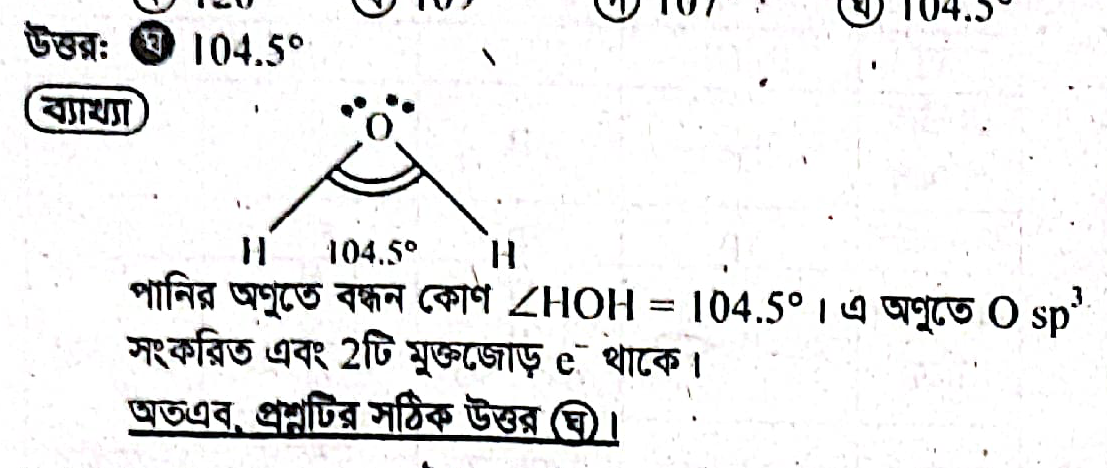
পানির অণুতে ∠HOH এর মান
পানির অণুতে ∠HOH এর মান 104.5°। এর কারণ নিচে ব্যাখ্যা করা হলো:
- কেন্দ্রীয় পরমাণু: পানির অণুতে অক্সিজেন (O) হলো কেন্দ্রীয় পরমাণু।
- ইলেকট্রন জোড়: অক্সিজেনের সর্ববহিঃস্থ স্তরে ৬টি ইলেকট্রন আছে। এটি হাইড্রোজেনের সাথে দুটি সমযোজী বন্ধন (covalent bond) তৈরি করে। ফলে অক্সিজেনের উপর দুটি বন্ধন জোড় (bond pair) এবং দুটি নিঃসঙ্গ ইলেকট্রন জোড় (lone pair) থাকে।

- VSEPR তত্ত্ব: ভ্যালেন্স শেল ইলেকট্রন পেয়ার রিপালশন (VSEPR) তত্ত্ব অনুযায়ী, ইলেকট্রন জোড়গুলো (বন্ধন জোড় ও নিঃসঙ্গ জোড়) নিজেদের মধ্যে বিকর্ষণ করে এবং যতটা সম্ভব দূরে থাকতে চায়।
- বিকর্ষণের ক্রম: নিঃসঙ্গ জোড় – নিঃসঙ্গ জোড় > নিঃসঙ্গ জোড় – বন্ধন জোড় > বন্ধন জোড় – বন্ধন জোড়। অর্থাৎ, নিঃসঙ্গ ইলেকট্রন জোড়ের মধ্যে বিকর্ষণ বন্ধন জোড়ের চেয়ে বেশি।
- আকৃতি: অক্সিজেনের উপর দুটি নিঃসঙ্গ ইলেকট্রন জোড় থাকায় এরা বন্ধন জোড়কে আরও বেশি বিকর্ষণ করে। ফলে ∠HOH এর মান আদর্শ চতুস্তলীয় কোণ 109.5° থেকে কমে 104.5° হয়। এর কারণে পানির অণুর আকৃতি কৌণিক (bent) হয়। 💧
গাণিতিকভাবে বিষয়টা এভাবে দেখানো যায়:
ধরা যাক, চতুস্তলীয় কোণ \( \theta_t = 109.5^\circ \)
নিঃসঙ্গ জোড়ের কারণে কোণ হ্রাস \( \Delta \theta \)
সুতরাং, \( \angle{HOH} = \theta_t - \Delta \theta = 104.5^\circ \) ✅
সারসংক্ষেপ: নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণের প্রভাবে পানির অণুর বন্ধন কোণ 104.5° হয়। 🎉
```


