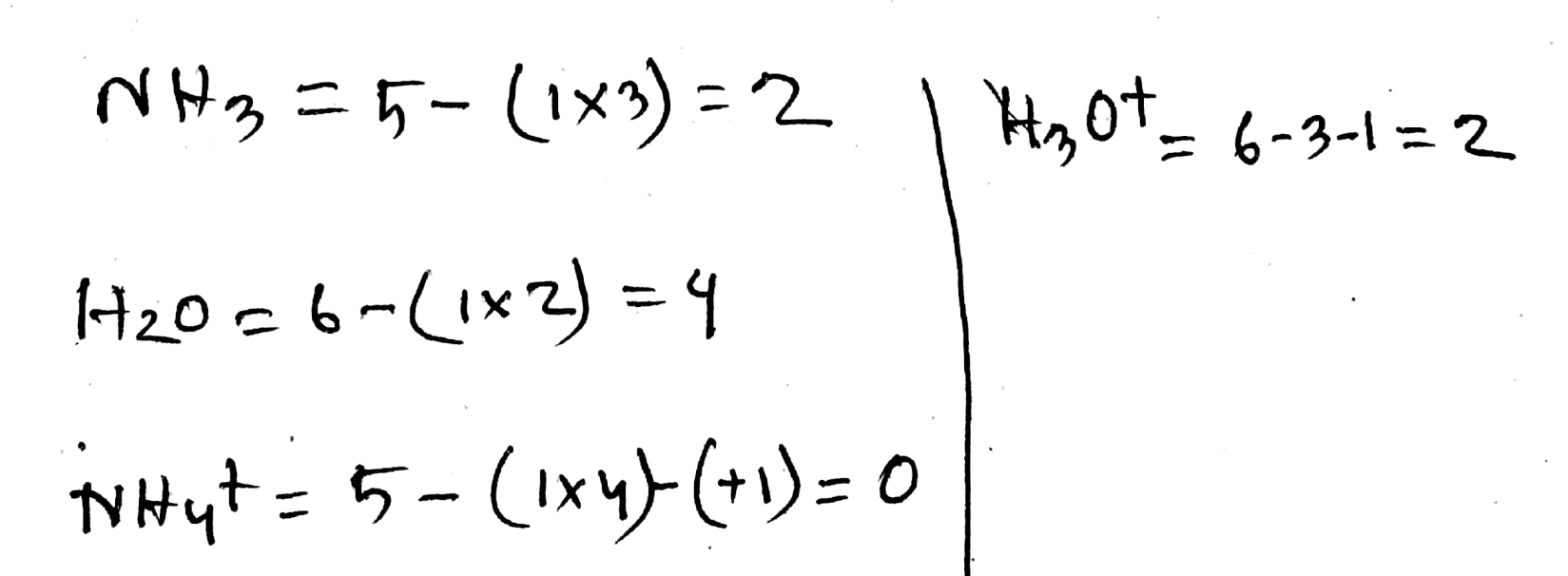Explanation:
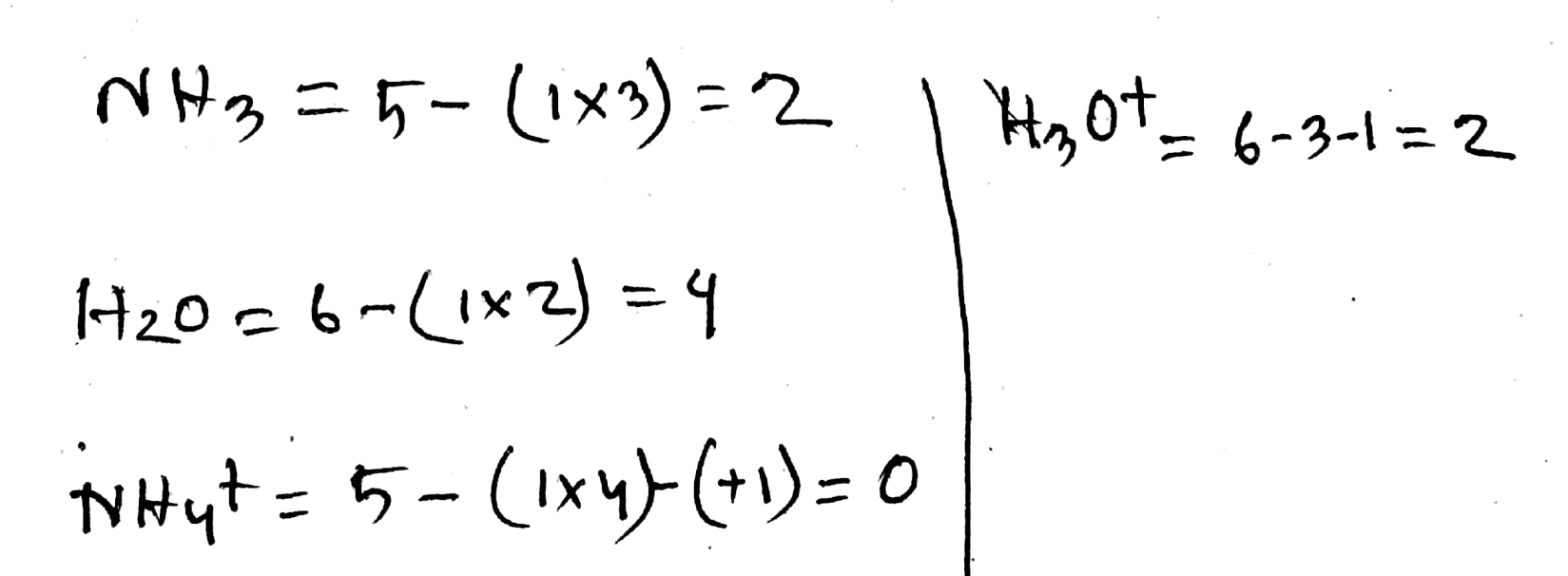
Another Explanation (5): ```html
কোনটিতে মুক্তজোড় ইলেকট্রনের প্রভাব সবচেয়ে বেশি: H2O এর ব্যাখ্যা
H2O (পানি)-তে মুক্তজোড় ইলেকট্রনের প্রভাব অন্যান্য অণুগুলোর তুলনায় বেশি হওয়ার কারণ নিচে আলোচনা করা হলো:
মুক্তজোড় ইলেকট্রন ও তাদের প্রভাব
- মুক্তজোড় ইলেকট্রন: কোনো পরমাণুর যোজ্যতা স্তরের (valence shell) যে ইলেকট্রনগুলো রাসায়নিক বন্ধন গঠনে অংশ নেয় না, সেগুলোকে মুক্তজোড় ইলেকট্রন বলে।
- প্রভাব: মুক্তজোড় ইলেকট্রনগুলো ঋণাত্মক চার্জযুক্ত হওয়ায় এরা অণুর আকার, আকৃতি, এবং রাসায়নিক বিক্রিয়া করার ক্ষমতাকে প্রভাবিত করে।
H2O-তে মুক্তজোড় ইলেকট্রনের প্রভাব বেশি হওয়ার কারণ
-
অক্সিজেনের দুটি মুক্তজোড় ইলেকট্রন: অক্সিজেন পরমাণুর যোজ্যতা স্তরে ৬টি ইলেকট্রন থাকে। এর মধ্যে ২টি হাইড্রোজেন পরমাণুর সাথে বন্ধন তৈরি করে এবং বাকি ৪টি (২ জোড়া) মুক্তজোড় ইলেকট্রন হিসেবে থাকে। 💧
-
তড়িৎ ঋণাত্মকতা (Electronegativity): অক্সিজেনের তড়িৎ ঋণাত্মকতা হাইড্রোজেন অপেক্ষা অনেক বেশি। ফলে অক্সিজেন বন্ধনের ইলেকট্রনগুলো নিজের দিকে বেশি টানে এবং আংশিক ঋণাত্মক চার্জ (δ-) প্রাপ্ত হয়।
-
আকৃতির উপর প্রভাব: দুটি মুক্তজোড় ইলেকট্রন জোড়ের কারণে জলের অণু সরলরৈখিক না হয়ে কৌণিক (bent) আকৃতির হয়। মুক্তজোড় ইলেকট্রনগুলো বন্ধন জোড় ইলেকট্রনকে বিকর্ষণ করে, ফলে বন্ধন কোণ ১০৯.৫° থেকে কমে ১০৪.৫° হয়।📐
-
পোলারিটি (Polarity): কৌণিক আকৃতি এবং অক্সিজেনের উচ্চ তড়িৎ ঋণাত্মকতার কারণে জলের অণু একটি পোলার অণু হিসেবে পরিচিত। এর ফলে জলের অণুতে একটি ধনাত্মক প্রান্ত (হাইড্রোজেন পরমাণু) এবং একটি ঋণাত্মক প্রান্ত (অক্সিজেন পরমাণু) সৃষ্টি হয়। ➕➖
-
হাইড্রোজেন বন্ধন (Hydrogen Bonding): জলের পোলারিটির কারণে একটি জলের অণু অন্য জলের অণুর সাথে হাইড্রোজেন বন্ধন তৈরি করতে পারে। এই বন্ধনের কারণে জলের স্ফুটনাঙ্ক (boiling point) অনেক বেড়ে যায়।🧊🔥
অন্যান্য অণুর সাথে তুলনা
| অণু (Molecule) |
মুক্তজোড় ইলেকট্রন সংখ্যা |
আকৃতি |
পোলারিটি |
মুক্তজোড় ইলেকট্রনের প্রভাব |
| H2O |
২ জোড়া |
কৌণিক (Bent) |
উচ্চ (High) |
অত্যধিক (Very High) ✅ |
| NH3 (অ্যামোনিয়া) |
১ জোড়া |
পিরামিডীয় (Pyramidal) |
মাঝারি (Moderate) |
মাঝারি (Moderate) |
| CH4 (মিথেন) |
০ |
চতুস্তলকীয় (Tetrahedral) |
অ-পোলার (Non-polar) |
নেই (None) |
উপরের তালিকা থেকে এটা স্পষ্ট যে, H2O-তে মুক্তজোড় ইলেকট্রনের সংখ্যা এবং এর পোলারিটির কারণে এর প্রভাব সবচেয়ে বেশি। 🤩
উপসংহার
পরিশেষে বলা যায়, H2O-এর কৌণিক গঠন, অক্সিজেনের উচ্চ তড়িৎ ঋণাত্মকতা এবং দুটি মুক্তজোড় ইলেকট্রন জোড়ের উপস্থিতির কারণে মুক্তজোড় ইলেকট্রনের প্রভাব অন্যান্য অণুগুলোর তুলনায় অনেক বেশি। এই প্রভাব জলের ভৌত ও রাসায়নিক ধর্মকে বিশেষভাবে প্রভাবিত করে। 👍
```