N
61.3%
49
সঠিক11
ভুল20
স্কিপ46.25
মোট মার্কস1
আলোকবর্ষ কিসের একক?
correct
ব্যাখ্যা:
আলোকবর্ষ দূরত্বের একক, কারণ এটি আলোর এক বছরে অতিক্রান্ত দূরত্ব। সঠিক উত্তর Option B। Option A: ভুল কারণ এটি সময় নির্দেশ করে। Option C এবং D: ভুল কারণ এরা অন্য পরিমাণ নির্দেশ করে। নোট: আলোকবর্ষ মহাকাশের বিশাল দূরত্ব পরিমাপের জন্য ব্যবহৃত হয়।
2
10 N মানের একটি বল X- অক্ষ বরাবর ক্রিয়া করলে Y অক্ষ বরাবর এর উপাংশ হবে-
skipped
ব্যাখ্যা:
বল \( 10 \, \text{N} \) X-অক্ষ বরাবর ক্রিয়াশীল। Y-অক্ষে উপাংশ হবে \( 10 \cos(90^\circ) = 0 \, \text{N} \)। সুতরাং সঠিক উত্তর D।
3
হাতঘড়ির কাঁটার কৌণিক বেগ ঘন্টার জন্য-
correct
ব্যাখ্যা:
ঘন্টা কাঁটার কৌণিক বেগ \( \omega = \frac{\theta}{t} = \frac{2\pi \, \text{radian}}{24 \times 3600 \, \text{seconds}} = \frac{\pi}{21600} \, \text{rads}^{-1} \)। সঠিক উত্তর: Option C। অন্য অপশনগুলো ভুল কারণ: A: ভুল, গণনা বড়। B: ভুল, গণনা ভুল। D: ভুল, সঠিক নয়। নোট: কৌণিক বেগ সময়ের সাথে ঘূর্ণন কোণের পরিবর্তন।
4
নিচের বলগুলোর মধ্যে কোনটি সবচেয়ে দুর্বল?
correct
ব্যাখ্যা:
বলগুলোর মধ্যে মহাকর্ষ বল সবচেয়ে দুর্বল।
5
5 kg ভর ও 0.5m চক্রগতির ব্যাসার্ধবিশিষ্ট একটি চাকা প্রতি মিনিটে 300 বার ঘুরছে। চাকাটির গতিশক্তি কত?
skipped
ব্যাখ্যা:
চাকার গতিশক্তি নির্ণয়: \( KE = \frac{1}{2}I\omega^2 \), যেখানে \( I = mr^2, \omega = \frac{2\pi N}{60} \), \( m = 5 \, \text{kg}, r = 0.25 \, \text{m}, N = 300 \)। সুতরাং, \( I = 5 \times (0.25)^2 = 0.3125 \, \text{kg} \cdot \text{m}^2, \omega = \frac{2\pi \times 300}{60} = 31.4 \, \text{rad/s} \)। অতএব, \( KE = \frac{1}{2} \times 0.3125 \times (31.4)^2 = 616.87 \, \text{J} \)। সঠিক উত্তর Option A। নোট: ঘূর্ণনশীল গতিশক্তি নির্ণয়ে \( KE = \frac{1}{2}I\omega^2 \) সূত্র ব্যবহার হয়।
6
6 N বল কোন বস্তুর উপর ক্রিয়া করায় বস্তুটি বলের দিকের সাথে ৬০° কোণ উৎপন্ন করে 10 m দূরে সরে গেল। কৃতকাজ কত?
correct
ব্যাখ্যা:
কৃতকাজ \( W = Fd\cos\theta = 6 \times 10 \times \cos 60^\circ = 30 \, \text{J} \)। সঠিক উত্তর Option D। অপশন বিশ্লেষণ: A: 6 J ভুল কারণ এটি বলের ভুল প্রয়োগ; B: 10 J ভুল কারণ এটি ভুল কোণের মানে ভিত্তি করে; C: 15 J ভুল কারণ এটি ভুল গাণিতিক ফলাফল। নোট: কাজ নির্ণয়ে \( W = Fd\cos\theta \) সূত্র ব্যবহার করা হয়।
7
একটি কণার ভরবেগ P। কণাটির গতিশক্তি দ্বিগুণ করলে এর নতুন ভরবেগ কত?
correct
ব্যাখ্যা:
কণার গতিশক্তি দ্বিগুণ করলে, ভরবেগ \( P \)-এর নতুন মান নির্ণয় করতে হবে। \( KE = \frac{P^2}{2m} \) অনুযায়ী, \( KE \) দ্বিগুণ হলে \( P \) হবে \( \sqrt{2}P \)।
8
\( g \)-এর মান কোথায় সর্বাধিক?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: \( g \)-এর মান যেখানে সর্বাধিক হবে তা সম্পর্কে জানতে চাওয়া হয়েছে। এটি পৃথিবীর মেরু অঞ্চলে সর্বাধিক হয়। অপশন বিশ্লেষণ: A. মেরু অঞ্চলে: সঠিক, এটি পৃথিবীর মেরু অঞ্চলে সর্বাধিক হয়। B. বিষুব রেখায়: ভুল, এটি সর্বাধিক নয়। C. ভূ-কেন্দ্রে: ভুল, এটি সঠিক নয়। D. ভূ-পৃষ্ঠ হতে অনেক দূরে: ভুল, এটি সঠিক নয়। নোট: পৃথিবীর মেরু অঞ্চলে \( g \)-এর মান সর্বাধিক হয়।
9
সমান ভরের দুটি উপগ্রহের ব্যাসার্ধ যথাক্রমে R এবং 4R হলে গ্রহ দুটির পর্যায় কালের অনুপাতঃ
skipped
ব্যাখ্যা:
সমান ভরের দুটি উপগ্রহের জন্য পর্যায় কালের অনুপাত \( T_1/T_2 = \sqrt{(R+4R)^3/R^3} \approx 0.047 \)। সঠিক উত্তর Option B। অন্য অপশনগুলো ভুল কারণ গণনা অনুযায়ী সঠিক মান নয়। নোট: কেপলারের সূত্র ব্যবহার করে উপগ্রহের পর্যায় কালের অনুপাত নির্ধারণ করা হয়।
10
তামার কাঠিন্যের গুনাঙ্ক \( n = ? \)
skipped
ব্যাখ্যা:
তামার কাঠিন্যের গুনাঙ্ক হলো বস্তুটির স্থিতিস্থাপকতার সাথে সম্পর্কিত। সঠিক উত্তরের জন্য কাঠিন্যের মান বা গুনাঙ্কের নির্দিষ্ট পরিমাণ নির্ধারিত থাকে যা নির্ভুল গণনায় পাওয়া যায়। অপশন A সঠিক কারণ তামার কাঠিন্যের গুনাঙ্ক \( 4 \times 10^{10} \, \text{Nm}^{-2} \)। অন্যান্য অপশন ভুল কারণ B (\( 5 \times 10^{10} \)), C (\( 6 \times 10^{10} \)), এবং D (\( 7 \times 10^{10} \)) মানটি সঠিক কাঠিন্যের গুনাঙ্ক থেকে বিচ্যুত। নোট: কাঠিন্যের গুনাঙ্ক নির্ধারণ বস্তুটির কাঠামোগত শক্তি এবং স্থিতিস্থাপকতার গুনানুপাত নির্দেশ করে।
11
একটি সরল দোলক 0.9s এ একবার টিক শব্দ করে।দোলকটির কার্যকর দৈর্ঘ্য কত?
skipped
ব্যাখ্যা:
সরল দোলকটির কার্যকর দৈর্ঘ্য \( l = \frac{gT^2}{4\pi^2} \) থেকে \( l \approx 0.80 \, \text{m} \)।
12
এক ঘনমিটার আয়তনের বায়ুতে যে পরিমাণ জলীয়বাষ্প থাকে, তা বায়ুর-
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এই প্রশ্নে বায়ুর আর্দ্রতা সম্পর্কিত প্রশ্ন করা হয়েছে। বায়ুতে যে পরিমাণ জলীয়বাষ্প থাকে, তা বায়ুর পরম আর্দ্রতার মাধ্যমে নির্ধারণ করা হয়। এটি তাপমাত্রা এবং আর্দ্রতার পরিমাণ অনুযায়ী পরিবর্তিত হতে পারে। অপশন বিশ্লেষণ: A. আর্দ্রতা: ভুল, এটি বায়ুর আর্দ্রতার একটি সাধারণ ধারণা, তবে এটি পরম আর্দ্রতা নয়। B. আপেক্ষিক আর্দ্রতা: ভুল, এটি কেবল আর্দ্রতার আপেক্ষিক পরিমাণ দেয় কিন্তু পরম আর্দ্রতা নয়। C. পরম আর্দ্রতা: সঠিক, এটি ঠিক সেই পরিমাণ জলীয়বাষ্প যা নির্দিষ্ট আয়তনে থাকতে পারে। D. কোনটিই নয়: ভুল, সঠিক উত্তর C। নোট: এই প্রশ্নের উত্তর পরম আর্দ্রতার সংজ্ঞা থেকে এসেছে, যা একটি নির্দিষ্ট আয়তনে কতটা জলীয়বাষ্প থাকতে পারে তা নির্দেশ করে।
13
0.20 kg রান্নার তেলের তাপমাত্রা 50°C বাড়াতে কত শক্তি প্রয়োজন,যদি এই তেলের আপেক্ষিক তাপ 1800 J/(kg°C)?
skipped
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এখানে রান্নার তেলের তাপমাত্রা বাড়ানোর জন্য প্রয়োজনীয় শক্তি নির্ধারণ করতে বলা হয়েছে। শক্তির হিসাব করতে তেলের আপেক্ষিক তাপ গুণ করতে হবে তাপমাত্রা পরিবর্তন এবং ভরের সাথে। অপশন বিশ্লেষণ: A. \(0.2 \times 50 \times 1800\): সঠিক, এটি সঠিক সমীকরণ অনুসরণ করে। B. \(0.2 \\times 50 \\times 1800\): ভুল, এতে সঠিক পরিমাপ নেই। C. \(1800 \cdot 0.2 \times 50\): ভুল, এটি সঠিক নয়। D. \(1800 \cdot 0.2 \times 50\): ভুল, এটি ভুল সমীকরণ। নোট: সমীকরণ অনুযায়ী, শক্তি হিসাব করার জন্য তেলের আপেক্ষিক তাপ গুণ করতে হবে ভর এবং তাপমাত্রা পরিবর্তনের সাথে।
14
100°C তাপমাত্রায় 2 kg পানিকে 100°C তাপমাত্রার বাষ্পে পরিণত করলে, এন্ট্রপির পরিবর্তন কত হয় নির্নয় কর?
incorrect
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: 100°C তাপমাত্রায় 2kg পানিকে বাষ্পে পরিণত করতে এন্ট্রপির পরিবর্তন কী হবে, তা নিয়ে প্রশ্ন করা হয়েছে। অপশন বিশ্লেষণ: A. 1.21 × 104 JK-1: সঠিক, এটি এন্ট্রপির সঠিক পরিবর্তন হিসেব করা হয়েছে। B. 1.21 × 105 JK-1: ভুল, এটি সঠিক নয়। C. 1.21 × 106 JK-1: ভুল, এটি অনেক বেশি। D. 1.21 × 107 JK-1: ভুল, এটি সঠিক নয়। নোট: এন্ট্রপির পরিবর্তন নির্ধারণে যে সূত্র ব্যবহার হয়েছে তা সঠিকভাবে প্রযোজ্য, যার মাধ্যমে সঠিক উত্তর পাওয়া গেছে।
15
পৃথিবীর তড়িৎ বিভব নিচের কোনটি?
incorrect
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এই প্রশ্নে পৃথিবীর তড়িৎ বিভব সম্পর্কিত জানতে চাওয়া হয়েছে। তড়িৎ বিভব হল একটি পয়েন্টের সাথে কোনো চার্জের সম্পর্কিত শক্তি। পৃথিবীর তড়িৎ বিভব ঋণাত্মক হলেও সাধারণত এটি নিরপেক্ষ হিসেবে বিবেচিত হয়। অপশন বিশ্লেষণ: A. ধনাত্মক: ভুল, পৃথিবীর তড়িৎ বিভব ধনাত্মক নয়। B. ঋণাত্মক: ভুল, পৃথিবীর তড়িৎ বিভব ঋণাত্মক নয়, এটি প্রায় শূন্য। C. অঋণাত্মক: ভুল, এটি পৃথিবীর তড়িৎ বিভবের সঠিক বর্ণনা নয়। D. কোনটিই নয়: সঠিক, পৃথিবীর তড়িৎ বিভবের মান প্রায় শূন্য। নোট: পৃথিবী একটি বিশাল আকারের বিদ্যুৎ ক্ষেত্র যার মধ্যে তড়িৎ বিভব প্রায় শূন্য হিসেবে বিবেচিত।
16
\( 1.34 \times 10^5 \, \text{N/C} \) প্রাবল্যের একটি তড়িৎ ক্ষেত্রে 15.8 cm ব্যবধানে অবস্থিত দুটি বিন্দুর বিভব পার্থক্য কত?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এখানে একটি তড়িৎ ক্ষেত্রে বিভব পার্থক্য বের করার জন্য কুলম্বের সূত্র ব্যবহার করা হয়েছে। প্রাবল্য \( 1.34 \times 10^5 \, \text{N/C} \) এবং দুটি বিন্দুর মধ্যে 15.8 cm দূরত্ব দেওয়া আছে। বিভব পার্থক্য বের করার জন্য \( V = E \times d \) সূত্র ব্যবহার করা হবে। অপশন বিশ্লেষণ: A. \( 2.12 \times 10^4 \, \text{V} \): সঠিক, এটি সমীকরণের মাধ্যমে সঠিক উত্তর। B. \( 2.12 \times 10^{-4} \, \text{V} \): ভুল, এটি সঠিক নয়। C. \( 1.12 \times 10^4 \, \text{V} \): ভুল, এটি সঠিক নয়। D. \( 1.12 \times 10^{-4} \, \text{V} \): ভুল, এটি সঠিক নয়। নোট: বিভব পার্থক্য বের করতে প্রাবল্য এবং দূরত্ব ব্যবহার করা হয়েছে এবং সঠিক উত্তর পাওয়া গেছে।
17
দুইটি গোলকের ব্যাসার্ধ যথাক্রমে 2 cm এবং 4 cm। এদেরকে যথাক্রমে 1000 কুলম্ব এবং 2000 কুলম্ব চার্জে চার্জিত করা হল। ক্ষুদ্র ও বৃহৎ গোলকের চার্জের তল ঘনত্বের অনুপাত কত?
skipped
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এখানে দুটি গোলকের ব্যাসার্ধ এবং চার্জের অনুপাত দেওয়া হয়েছে। গোলকের ব্যাসার্ধ এবং চার্জের অনুপাত দিয়ে, গোলকের তল ঘনত্বের অনুপাত বের করা হবে। এটি কুলম্ব সূত্রের মাধ্যমে সমাধান করা হবে। অপশন বিশ্লেষণ: A. 2:01: সঠিক, এটি কুলম্ব সূত্র অনুযায়ী সঠিক উত্তর। B. 1:02: ভুল, এটি ভুল অনুপাত। C. 4:01: ভুল, এটি ভুল অনুপাত। D. 1:04: ভুল, এটি ভুল অনুপাত। নোট: গোলকের তল ঘনত্বের অনুপাত কুলম্ব সূত্রের মাধ্যমে বের করা হয়েছে।
18
একটি তারের কুন্ডলীর ক্ষেত্রফল \(2×10^{-4} \, \text{m}^2\) এবং কুন্ডলীর মধ্য দিয়ে \(0.01 \, \text{A}\) বিদ্যুৎ প্রবাহ চললে কুন্ডলীর দ্বিপোল মোমেন্ট কত?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এই প্রশ্নে কুন্ডলীর দ্বিপোল মোমেন্ট বের করার জন্য প্রশ্ন করা হয়েছে। কুন্ডলীর ক্ষেত্রফল এবং বিদ্যুৎ প্রবাহ জানিয়ে দেয়া হয়েছে। দ্বিপোল মোমেন্ট বের করার জন্য সমীকরণ \( m = A \cdot I \cdot L \) ব্যবহার করতে হবে। অপশন বিশ্লেষণ: A. \( 2×10^{-6} \, \text{Am} \): ভুল, এটি সঠিক নয়। B. \( 2×10^{-5} \, \text{Am}^2 \): ভুল, এটি সঠিক নয়। C. \( 2×10^{-6} \, \text{Am}^2 \): সঠিক, এটি সঠিক সমীকরণের ভিত্তিতে বের করা হয়েছে। D. \( 2×10^{-6} \, \text{A}^2\text{m}^2 \): ভুল, এটি সঠিক নয়। নোট: দ্বিপোল মোমেন্টের সমীকরণ ব্যবহার করে সঠিক উত্তর পাওয়া গেছে।
19
1.5 m দূরে অবস্থিত পর্দায় পরস্পর থেকে 0.03 cm দূরত্বে ডোরা তৈরি হলো। কেন্দ্রীয় চরম থেকে 1 cm দূরে চতুর্থ উজ্জ্বল ডোরাটি হলো। আলোর তরঙ্গদৈর্ঘ্য নির্ণয় কর।
skipped
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এই প্রশ্নে ডোরার দূরত্ব এবং কেন্দ্রীয় চরম থেকে নির্দিষ্ট দূরত্বের ডোরার অবস্থান নিয়ে আলোর তরঙ্গদৈর্ঘ্য বের করার কথা বলা হয়েছে। প্রথমে ডোরার দূরত্ব এবং তাদের অবস্থান ব্যবহার করে তরঙ্গদৈর্ঘ্য বের করার জন্য ডবল স্লিট এক্সপেরিমেন্টের সূত্র ব্যবহার করতে হবে। অপশন বিশ্লেষণ: A. 2500 Å: ভুল, এটি সঠিক তরঙ্গদৈর্ঘ্য নয়। B. 5000 Å: সঠিক, এটি তরঙ্গদৈর্ঘ্য নির্ণয়ের জন্য সঠিক মান। C. 6000 Å: ভুল, এটি সঠিক তরঙ্গদৈর্ঘ্য নয়। D. 7500 Å: ভুল, এটি সঠিক নয়। নোট: ডবল স্লিটের সূত্র ব্যবহার করে আলোর তরঙ্গদৈর্ঘ্য বের করা হয়েছে, যেখানে কেন্দ্র থেকে ডোরার অবস্থান এবং ডোরার দূরত্বের ভিত্তিতে 5000 Å প্রাপ্ত হয়েছে।
20
কোন তরঙ্গের সমবর্তন হয় না?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এই প্রশ্নে তরঙ্গের সমবর্তন সম্পর্কে জানতে চাওয়া হয়েছে। তরঙ্গের সমবর্তন হলে তা উপাদানের মাধ্যমে শক্তি স্থানান্তর করে, কিন্তু কিছু তরঙ্গের ক্ষেত্রে সমবর্তন ঘটে না। অপশন বিশ্লেষণ: A. এক্স-রশ্মি: ভুল, এক্স-রশ্মি একটি ট্রান্সভার্স তরঙ্গ যা সমবর্তন হয় না। B. শব্দ তরঙ্গ: সঠিক, শব্দ তরঙ্গ সমবর্তন হয়। C. রেডিও তরঙ্গ: ভুল, রেডিও তরঙ্গ সমবর্তন হয়। D. সাধারণ আলো: ভুল, আলোও সমবর্তন হয়। নোট: শব্দ তরঙ্গ সমবর্তন হয় না কারণ এটি একটি লম্বালম্বি তরঙ্গ যা সমবর্তন ঘটাতে পারে না।
21
অন্ধকারে ছবি তোলার জন্য ___ক্যামেরা ব্যাবহার করা হয়।
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: অন্ধকারে ছবি তোলার জন্য ব্যবহৃত রশ্মি সম্পর্কে প্রশ্ন করা হয়েছে। অপশন বিশ্লেষণ: A. গামা রশ্মি: ভুল, এটি ব্যবহৃত হয় না। B. অতিবেগুনী: ভুল, এটি ব্যবহৃত হয় না। C. এক্স-রশ্মি: ভুল, এটি ব্যবহৃত হয় না। D. অবলোহিত রশ্মি: সঠিক, এটি অন্ধকারে ছবি তোলার জন্য ব্যবহৃত হয়। নোট: অবলোহিত রশ্মি অন্ধকারে ছবি তোলার জন্য সবচেয়ে উপযুক্ত।
22
নিচের কোনটি গামা রশ্মির ধর্ম হবে?
incorrect
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এখানে গামা রশ্মির ধর্ম সম্পর্কে প্রশ্ন করা হয়েছে। গামা রশ্মি একটি উচ্চ শক্তির রশ্মি, যার ভেদন ক্ষমতা রয়েছে এবং এটি পদার্থের ভেদ করার ক্ষমতা রাখে। অপশন বিশ্লেষণ: A. এটি হালকা: ভুল, গামা রশ্মির বর্ণালী ঠিক হালকা নয়। B. এর ভেদন ক্ষমতা আছে: সঠিক, গামা রশ্মির ভেদন ক্ষমতা রয়েছে। C. এর গতিশক্তি আছে: সঠিক, গামা রশ্মির গতিশক্তি থাকে। D. এর ভর নেই: সঠিক, গামা রশ্মির ভর নেই। নোট: গামা রশ্মি অত্যন্ত শক্তিশালী এবং ভেদ করার ক্ষমতা রাখে, যার কারণে এটি হালকা নয়।
23
কোন বস্তুর প্রতি সেকেন্ডে একটি পরমাণুর ভাঙ্গনকে বলে-
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: পরমাণুর ভাঙ্গনকে বেকেরেল দ্বারা পরিমাপ করা হয়, এবং 1 বেকেরেল মানে প্রতি সেকেন্ডে একটি পরমাণুর ভাঙ্গন। অপশন বিশ্লেষণ: A. 1 বেকেরেল: সঠিক, এটি সঠিক সংজ্ঞা। B. 1 ফ্যারাডে: ভুল, এটি ভুল একক। C. 1 হেনরী: ভুল, এটি ভুল একক। D. 1 কুরী: ভুল, এটি ভুল একক। নোট: এই প্রশ্নে পরমাণু ভাঙ্গনকে পরিমাপের জন্য সঠিক একক ব্যবহার করা হয়েছে।
24
বিশুদ্ধতম আকারে একটি অর্ধপরিবাহীকে বলা হয়ঃ
skipped
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এই প্রশ্নে বিশুদ্ধতম আকারে একটি অর্ধপরিবাহী সম্পর্কে জানতে চাওয়া হয়েছে। সঠিক উত্তর হলো সহজাত অর্ধপরিবাহী, যেটি সিলিকন ও জার্মেনিয়ামের মতো মৌলগুলির জন্য প্রযোজ্য। অপশন বিশ্লেষণ: A. অন্তরক: ভুল, এটি অর্ধপরিবাহী নয়। B. সুপার কন্ডাকটর: ভুল, এটি একধরনের উপাদান যা বিশেষ অবস্থায় তাপমাত্রা নিচে গেলে বিদ্যুৎ পরিবহন করতে পারে। C. সহজাত অর্ধপরিবাহী: সঠিক, এটি বিশুদ্ধতম আকারে অর্ধপরিবাহী। D. বহির্জাত অর্ধপরিবাহী: ভুল, এটি সমানভাবে বিশুদ্ধ নয়। E. --: অপশন নেই। নোট: সহজাত অর্ধপরিবাহী হলো বিশুদ্ধতম আকারে অর্ধপরিবাহী।
25
কোন প্রক্রিয়াটি তরল যৌগের বিশোধনের জন্য ব্যবহার করা হয়?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: তরল যৌগ বিশোধনের জন্য পাতন প্রক্রিয়া ব্যবহৃত হয়। অপশন বিশ্লেষণ: A. কেলাসন: ভুল, এটি ধাতব আয়নের সাথে জৈব যৌগ যুক্ত করার পদ্ধতি। B. পাতন: সঠিক, তরল যৌগ পৃথকীকরণের জন্য এটি ব্যবহৃত হয়। C. উর্ধ্বপাতন: ভুল, এটি কঠিন পদার্থের জন্য ব্যবহৃত হয়। D. পরিস্রাবণ: ভুল, এটি কঠিন ও তরল পৃথকীকরণে ব্যবহৃত হয়। নোট: পাতন প্রক্রিয়া তরল পদার্থ পৃথকীকরণে একটি মৌলিক পদ্ধতি।
26
পরমাণুস্থ কোন ইলেকট্রনের জন্য কোয়ান্টাম সংখ্যার কোন সেটটি সম্ভব নয়?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: ইলেকট্রনের কোয়ান্টাম সংখ্যাগুলির মধ্যে n (প্রধান কোয়ান্টাম সংখ্যা), l (কৌণিক গতিশক্তির কোয়ান্টাম সংখ্যা), m (চৌম্বকীয় কোয়ান্টাম সংখ্যা), এবং s (স্পিন কোয়ান্টাম সংখ্যা) এর মান নির্দিষ্ট নিয়ম মেনে চলতে হয়। এখানে n এর মান l এর চেয়ে বড় হতে হবে এবং l এর মান সর্বোচ্চ \(n-1\) হতে পারে। অপশন বিশ্লেষণ: Option A: n = 3, l = 3, m = 1, s = -1/2 — ভুল, কারণ l = 3 হলে এটি \(n-1\) হতে পারে না। n = 3 হলে l এর মান হতে পারে 0, 1, বা 2। Option B: n = 2, l = 1, m = 0, s = 1/2 — সঠিক, এটি নিয়মের মধ্যে পড়ে। Option C: n = 4, l = 3, m = -1, s = -1/2 — সঠিক, এটি নিয়মের মধ্যে পড়ে। Option D: n = 4, l = 3, m = 1, s = -1/2 — সঠিক, এটি নিয়মের মধ্যে পড়ে। নোট: ইলেকট্রনের কোয়ান্টাম সংখ্যা নির্বাচন করতে গেলে অবশ্যই কোয়ান্টাম সংখ্যা সেটের মধ্যে সম্পর্ক বুঝে সঠিকভাবে যাচাই করতে হবে।
27
সবুজ আলোর তরংগ দৈর্ঘ্য কত?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: সবুজ আলোর তরঙ্গদৈর্ঘ্য সাধারণত ৫০০-৫৭৫ nm এর মধ্যে। এটি দৃশ্যমান আলোর মধ্যবর্তী অংশ। অপশন বিশ্লেষণ: A. 425-450 nm: ভুল, এটি নীল রঙের তরঙ্গদৈর্ঘ্য। B. 500-575 nm: সঠিক, এটি সবুজ আলোর সঠিক তরঙ্গদৈর্ঘ্য। C. 450-500 nm: ভুল, এটি সবুজের চেয়ে ছোট তরঙ্গদৈর্ঘ্য। D. 625-780 nm: ভুল, এটি লাল রঙের তরঙ্গদৈর্ঘ্য। নোট: সবুজ আলোর তরঙ্গদৈর্ঘ্য পরিবেশ এবং জীববিজ্ঞানীয় বিভিন্ন প্রক্রিয়ার জন্য গুরুত্বপূর্ণ।
28
নিম্নের কোনটিতে হাইড্রোজেন বন্ধন বিদ্যমান?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: হাইড্রোজেন বন্ধন বিদ্যমান অণু নির্ণয় করতে বলা হয়েছে। C6H5COOH (বেনজয়িক অ্যাসিড) অণুতে -OH এবং C=O-এর মধ্যে আন্তঃআণবিক হাইড্রোজেন বন্ধন বিদ্যমান। অপশন বিশ্লেষণ: A. C6H5COOH: সঠিক, এতে হাইড্রোজেন বন্ধন বিদ্যমান। B. H2S: ভুল, এতে হাইড্রোজেন বন্ধন নেই। C. CS2: ভুল, এতে কোনো হাইড্রোজেন পরমাণু নেই। D. কোনটিই নয়: ভুল, সঠিক উত্তর আছে। নোট: হাইড্রোজেন বন্ধনের জন্য H এবং একটি উচ্চ ইলেকট্রনেগেটিভ পরমাণু (F, O, N) প্রয়োজন।
29
তড়িৎ ঋণাত্মকতা অনুযায়ী হ্যালোজেন মৌলসমূহের সঠিক ক্রম কোনটি?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: তড়িৎ ঋণাত্মকতার ক্রম হ্যালোজেন মৌলসমূহের জন্য নির্ধারণ করতে বলা হয়েছে। তড়িৎ ঋণাত্মকতা হলো ইলেকট্রন আকর্ষণের ক্ষমতা। হ্যালোজেনগুলির ক্রম \( F > Cl > Br > I \), কারণ ফ্লুওরিনের আকর্ষণ ক্ষমতা সর্বোচ্চ। অপশন বিশ্লেষণ: A: ভুল, কারণ এটি সঠিক ক্রম নয়। B: ভুল, এটি উল্টো ক্রম। C: সঠিক, কারণ \( F > Cl > Br > I \)। D: ভুল, কারণ ক্রমের মধ্যে ভুল রয়েছে। নোট: তড়িৎ ঋণাত্মকতার ???্রম মৌলের আয়নীয় এবং যৌগিক আচরণ নির্ধারণে সহায়ক।
30
বক্সাইট আকরিকের সংকেত কি?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: বক্সাইট হলো অ্যালুমিনিয়ামের একটি আকরিক, যার সংকেত হলো \(Al_2O_3·2H_2O\)। এটি অ্যালুমিনিয়াম নিষ্কাশনের প্রধান উৎস। অপশন বিশ্লেষণ: A. \(Al_2O_3·2H_2O\): সঠিক, এটি বক্সাইটের সংকেত। B. \(CaO.SiO_2\): ভুল, এটি সিমেন্টের উপাদান। C. \(CaSO_3·2H_2O\): ভুল, এটি জিপসামের সংকেত। D. \(CaSO_3\): ভুল, এটি সঠিক নয়। নোট: বক্সাইট অ্যালুমিনিয়াম নিষ্কাশনে অত্যন্ত গুরুত্বপূর্ণ আকরিক।
31
কোনটি নিরপেক্ষ অক্সাইড?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: নিরপেক্ষ অক্সাইড চিহ্নিত করতে বলা হয়েছে। নিরপেক্ষ অক্সাইড বিদ্যুৎ পরিবহন করে না এবং জলে দ্রবীভূত হয়ে কোনো এসিড বা ক্ষার তৈরি করে না। অপশন বিশ্লেষণ: A. NO2: ভুল, এটি অ্যাসিডিক। B. N2O: সঠিক, এটি নিরপেক্ষ। C. N2O5: ভুল, এটি অ্যাসিডিক। D. SO5: ভুল, এটি অক্সাইড নয়। নোট: নিরপেক্ষ অক্সাইডের বৈশিষ্ট্য হলো তারা রাসায়নিকভাবে নিষ্ক্রিয়।
32
কোন যৌগে হাইড্রোজেন বন্ধন আছে?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এখানে হাইড্রোজেন বন্ধনযুক্ত যৌগ খুঁজতে বলা হয়েছে। হাইড্রোজেন বন্ধন সাধারণত OH বা NH গ্রুপের উপস্থিতিতে তৈরি হয়। ফেনলে \( -OH \) গ্রুপ থাকে, তাই এটি হাইড্রোজেন বন্ধনযুক্ত। অপশন বিশ্লেষণ: Option A: সঠিক, কারণ ফেনল একটি \( -OH \) গ্রুপ ধারণ করে। Option B: ভুল, কারণ বেনজালডিহাইডে হাইড্রোজেন বন্ধনের জন্য প্রয়োজনীয় \( -OH \) গ্রুপ নেই। Option C: ভুল, কারণ বেনজিনে কোনো ফাংশনাল গ্রুপ নেই যা হাইড্রোজেন বন্ধন তৈরি করতে পারে। Option D: ভুল, নাইট্রোমিথেনে হাইড্রোজেন বন্ধনের উপযুক্ত গঠন নেই। নোট: হাইড্রোজেন বন্ধনের জন্য প্রয়োজনীয় গ্রুপ এবং তাদের গঠনের বিষয়ে সতর্ক থাকতে হবে।
33
কোন জলীয় দ্রবনেটিতে হাইড্রোক্সাইড আয়নের ঘনমাত্রা সর্বনিম্ন?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: হাইড্রোক্সাইড আয়নের ঘনমাত্রা \(pH\)-এর সাথে সম্পর্কযুক্ত এবং \(pH\)-এর মান বেশি হলে হাইড্রোক্সাইড আয়নের ঘনমাত্রা কম হয়। \(pH=4\) (H₂SO₄ দ্রবণ) এ হাইড্রোক্সাইড আয়নের ঘনমাত্রা সর্বনিম্ন। অপশন বিশ্লেষণ: A. HCl (\(pH=1\)): ভুল, এতে হাইড্রোক্সাইড আয়ন বেশি। B. CH₂COOH (\(pH=0.1\)): ভুল, এটি শক্তিশালী অ্যাসিড নয়। C. H₂SO₄ (\(pH=4\)): সঠিক, এটি হাইড্রোক্সাইড আয়নের সর্বনিম্ন ঘনমাত্রা। D. HNO₃ (\(pH=1.5\)): ভুল, হাইড্রোক্সাইড আয়ন বেশি। নোট: এই প্রশ্নটি অ্যাসিড ও বেসের প্রকৃতি বোঝার জন্য অত্যন্ত সহায়ক।
34
#NAME?
skipped
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এই প্রশ্নে প্রশ্ন করা হয়েছে কোন যৌগটি একটি সঠিক আধান প্রদান করে। অপশন বিশ্লেষণ: A. AH₃O⁺: ভুল, এটি সাধারণত কোন প্রযোজ্য আধান সম্পর্কিত নয়। B. H₂O: সঠিক, পানি (H₂O) একটি নিরপেক্ষ অণু যা আধান প্রদান করে। C. O₂⁻: ভুল, এটি অক্সিজেন আধানযুক্ত আণু হলেও সঠিক উত্তর নয়। D. O₂: ভুল, অক্সিজেন আণু আধান প্রদান করবে না। নোট: এই প্রশ্নে সঠিক আধান সৃষ্টিকারী যৌগের মধ্যে পানির ভূমিকা বিশেষভাবে চিহ্নিত হয়েছে।
35
একটি দ্রবণের pH=3.61 হলে দ্রবণটির [H3O+] কত?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: \(pH = -\log[H_3O^+]\) সূত্র থেকে [H₃O⁺] নির্ণয় করা যায়। \(pH = 3.61\) হলে, \([H_3O^+] = 10^{-3.61} = 2.51 \times 10^{-4} \, \text{mol/dm³}\)। অপশন বিশ্লেষণ: A. \(2.51 \times 10^{-3} \, \text{mol/dm³}\): ভুল, দশমিক বিন্যাস ত্রুটি। B. \(2.51 \times 10^{-4} \, \text{mol/dm³}\): সঠিক, সঠিক মান। C. \(2.51 \times 10^2 \, \text{mol/dm³}\): ভুল, ভুল নির্দেশনা। D. \(0.215 \times 10^5 \, \text{mol/dm³}\): ভুল, অনুপযুক্ত বিন্যাস। নোট: \(pH\)-এর ভিত্তিতে \(H_3O^+\)-এর ঘনমাত্রা নির্ণয় রসায়নে অত্যন্ত গুরুত্বপূর্ণ।
36
খাদ্যের পচন ঘটার কারণ- \( (i) \) খাদ্যে পানি থাকা \( (ii) \) ছত্রাক জন্মানো, \( (iii) \) তাপমাত্রা \(45^\circ C\) এর বেশি থাকা । নিচের কোনটি সঠিক ?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: খাদ্যের পচন পানির উপস্থিতি, ছত্রাকের বৃদ্ধি এবং উচ্চ তাপমাত্রার জন্য ঘটে। অপশন বিশ্লেষণ: A: i, ii: ভুল, কারণ এটি সব কারণ অন্তর্ভুক্ত করেনি। B: i, iii: ভুল, কারণ এটি ছত্রাক বাদ দিয়েছে। C: ii, iii: ভুল, কারণ এটি পানি বাদ দিয়েছে। D: i, ii, iii: সঠিক, কারণ সব কারণ উপস্থিত। নোট: খাদ্যের সংরক্ষণে সব কারণ নিয়ন্ত্রণে রাখা প্রয়োজন।
37
CO2 গ্যাসের ক্রান্তি তাপমাত্রা হলো -
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: CO2 গ্যাসের ক্রান্তি তাপমাত্রা হলো সেই তাপমাত্রা যেখানে CO2 তরল ও গ্যাসীয় অবস্থার মধ্যে পরিবর্তন ঘটায়। এটি হলো 31.1°C। অপশন বিশ্লেষণ: A. 31.1°C: সঠিক, এটি CO2 এর ক্রান্তি তাপমাত্রা। B. 118.8°C: ভুল, এটি খুব বেশি। C. -240°C: ভুল, এটি ক্রান্তি তাপমাত্রার পরিসরে নেই। D. 48.1°C: ভুল, এটি CO2 এর জন্য সঠিক নয়। নোট: ক্রান্তি তাপমাত্রার উপরে CO2 গ্যাস হিসেবে থাকে এবং তরলে পরিণত হতে পারে না।
38
ভূমিকম্পনের ফলে সৃষ্ট তরঙ্গ হলো-
incorrect
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: ভূমিকম্পের ফলে সৃষ্ট তরঙ্গ সম্পর্কে প্রশ্ন করা হয়েছে। অপশন বিশ্লেষণ: A. আড় তরঙ্গ: সঠিক, ভূমিকম্পের মূল তরঙ্গ হলো আড় তরঙ্গ। B. লাম্বিক তরঙ্গ: ভুল, এটি ভূমিকম্পের পৃষ্ঠীয় তরঙ্গ। C. আড় ও লম্বিক তরঙ্গের মিশ্রণ: ভুল, এটি সঠিক নয়। D. কোনটিই নয়: ভুল, আড় তরঙ্গ সঠিক উত্তর। নোট: ভূমিকম্পের ফলে আড় তরঙ্গ প্রথমে সৃষ্টি হয়, এটি ভূগর্ভের মাধ্যমে দ্রুত যাত্রা করে।
39
ঘূর্ণিঝড় সৃষ্টির জন্য পানির তাপমাত্রা কত °C এর উপর থাকতে হয়?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: ঘূর্ণিঝড় ???ৃষ্টির জন্য পানির তাপমাত্রা একটি গুরুত্বপূর্ণ বিষয়। ঘূর্ণিঝড় তখনই সৃষ্টি হয় যখন সামুদ্রিক পানির তাপমাত্রা কমপক্ষে 27°C বা তার বেশি হয়, কারণ এই তাপমাত্রায় প্রচুর বাষ্পায়ন ঘটে যা ঘূর্ণিঝড়ের শক্তির উৎস। অপশন বিশ্লেষণ: A: 25°C, ভুল, এই তাপমাত্রা ঘূর্ণিঝড় সৃষ্টির জন্য যথেষ্ট নয়। B: 27°C, স???িক, এই তাপমাত্রা ঘূর্ণিঝড় সৃষ্টির ন্যূনতম প্রয়োজনীয় তাপমাত্রা। C: 40°C, ভুল, এটি অত্যন্ত বেশি এবং বাস্তবে এমন পানির তাপমাত্রা পাওয়া যায় না। D: 30°C, ভুল, যদিও এটি উচ্চ তাপমাত্রা, কিন্তু প্রশ্নে ন্যূনতম তাপমাত্রার কথা বলা হয়েছে। নোট: ঘূর্ণিঝড় সৃষ্টির জন্য পানির তাপমাত্রা 27°C হতে হবে এবং এটি অধিকাংশ ক্ষেত্রে গ্রীষ্মমন্ডলীয় অঞ্চলে ঘটে।
40
RCOOH + ROH \\( \\xrightarrow{H_2SO_4} \\) A + H2O; A যৌগটি হচ্ছে
skipped
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: প্রদত্ত বিক্রিয়ায় এসিড (RCOOH) এবং অ্যালকোহল (ROH) এর বিক্রিয়ায় গঠিত যৌগটি একটি এস্টার। অপশন বিশ্লেষণ: A. অ্যামিন: ভুল, এটি নাইট্রোজেনযুক্ত যৌগ। B. অ্যামাইড: ভুল, এটি অ্যামিনো অ্যাসিড হতে গঠিত হয়। C. এস্টার: সঠিক, এটি এসিড এবং অ্যালকোহলের বিক্রিয়ায় উৎপন্ন হয়। D. অ্যানহাইড্রাইড: ভুল, এটি শুধুমাত্র এসিডের বিক্রিয়ায় উৎপন্ন হয়। নোট: এস্টার গঠন একটি গুরুত্বপূর্ণ জৈব রাসায়নিক বিক্রিয়া এবং সুগন্ধি পদার্থের জন্য ব্যবহৃত হয়।
41
বেনজাইল ক্লোরাইড এর গাঠনিক সংকেত কোনটি?
skipped
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: বেনজাইল ক্লোরাইডের গঠন নির্ধারণ করতে হবে। এটি C6H5-CH2Cl আকারে থাকে। অপশন বিশ্লেষণ: A. ভুল, এটি বেনজাইল ক্লোরাইড নয়। B. সঠিক, এটি বেনজাইল ক্লোরাইডের গঠন। C. ভুল, এটি ভুল গঠন। D. ভুল, এটি ভুল গঠন। নোট: বেনজাইল ক্লোরাইডের গঠন তার নির্ধারিত বৈশিষ্ট্যের জন্য গুরুত্বপূর্ণ।
42
CH3-CH2CH(CH3)-CH(C2H5)2 যৌগটির IUPAC নাম?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: যৌগটির শৃঙ্খল বিশ্লেষণ করে IUPAC নামকরণ করতে হয়। প্রধান শৃঙ্খলটি হেক্সেন, এবং এতে ৩ নম্বর কার্বনে মিথাইল এবং ৪ নম্বর কার্বনে ইথাইল গ্রুপ আছে। অপশন বিশ্লেষণ: A. সঠিক, কারণ IUPAC নিয়ম অনুসারে এটি সঠিক নাম। B. ভুল, কারণ গ্রুপগুলোর অবস্থান ভুল। C. ভুল, কারণ এটি ভুল নাম। D. ভুল, কারণ এটি সঠিক নাম নয়। নোট: IUPAC নামকরণের নিয়ম অনুসরণ করলে যৌগের সঠিক নাম নির্ধারণ করা যায়।
43
বেনজ্যামাইডের মাধ্যমে হফম্যান ক্ষুদ্রাংশকরণ বিক্রিয়ায় তৈরি প্রধান উৎপাদের সাথে নাইট্রাস এসিড উত্তপ্ত অবস্থায় কি উৎপন্ন করে?
incorrect
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: বেনজ্যামাইডের মাধ্যমে হফম্যান ক্ষুদ্রাংশকরণ বিক্রিয়ায় তৈরি প্রধান উৎপাদ হলো অ্যানিলিন। নাইট্রাস এসিডের সাথে উত্তপ্ত অবস্থায় এটি বেনজিন ডায়াজোনিয়াম ক্লোরাইড উৎপন্ন করে। অপশন বিশ্লেষণ: A. বেনজিন ডায়াজোনিয়াম ক্লোরাইড: সঠিক, এটি প্রধান উৎপাদ। B. ফিনাইল কার্বিল অ্যামিন: ভুল, এটি পার্শ্ব বিক্রিয়া হতে পারে। C. নাইট্রোবেনজিন: ভুল, এটি সংশ্লিষ্ট নয়। D. ফেনল: ভুল, এটি পরবর্তী পদক্ষেপে উৎপন্ন হতে পারে। নোট: হফম্যান ক্ষুদ্রাংশকরণ গুরুত্বপূর্ণ কারণ এটি নাইট্রোজেনযুক্ত যৌগ উৎপাদনে ব্যবহৃত হয়।
44
কোন যৌগটি জ্যামিতিক সমাণুতা প্রদর্শন করে না?
incorrect
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: প্রশ্নে একটি জ্যামিতিক সমানুতা প্রদর্শন না করা যৌগ জানতে চাওয়া হয়েছে। অপশন বিশ্লেষণ: A. CH3−HC=CH−Cl: সঠিক, এটি একটি জ্যামিতিক সমানুতা প্রদর্শন করে (সি=সি বন্ধন)। B. CH3-HC=CCl-Cl: ভুল, এটি সঠিক নয়, কারণ দুটি ক্লোরিন আয়ন একই দিকে অবস্থান করছে, যা জ্যামিতিক সমানুতা প্রদর্শন করে না। C. CH3-HC=CH-CH3: সঠিক, এটি জ্যামিতিক সমানুতা প্রদর্শন করে (সি=সি বন্ধন)। D. CH3-CCl=CH-Cl: সঠিক, এটি জ্যামিতিক সমানুতা প্রদর্শন করে। নোট: জ্যামিতিক সমানুতা কোনো রাসায়নিক যৌগের সি=সি বন্ধন থাকা উচিত যেখানে আণবিক গ্রুপগুলি কিছু নির্দিষ্ট দিকে অবস্থান করে।
45
6 গ্রাম কার্বনে কয়টি কার্বন পরমাণু থাকবে?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: এখানে 6 গ্রাম কার্বনে কতটি কার্বন পরমাণু থাকবে তা জানতে চাওয়া হয়েছে। এটা মূলত মৌলিক পরমাণু সংখ্যা সম্পর্কে প্রশ্ন। 6 গ্রাম কার্বনের মধ্যে 1 মোল কার্বন থাকে, যা \(6.023 \times 10^{23}\) পরমাণু। অপশন বিশ্লেষণ: A. \(6.023 \times 10^{23}\): সঠিক, এটি 1 মোল পরমাণুর সংখ্যা। B. \(3.012 \times 10^{-23}\): ভুল, এটি সঠিক নয়। C. \(3.012 \times 10^{23}\): সঠিক, এটি 6 গ্রাম কার্বনের জন্য সঠিক সংখ্যা। D. কোনটিই নয়: ভুল, সঠিক উত্তর দেওয়া হয়েছে। নোট: এই প্রশ্নে আণবিক ভর এবং মোল ধারণা ব্যবহার করা হয়েছে।
46
জারণ বিজারন বিক্রিয়ায় KMnO4 যখন Mn2+ এ পরিবর্তীত হয়, তখন Mn মৌলটি-
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: জারণ বিজারন বিক্রিয়ার মাধ্যমে KMnO4 থেকে Mn2+ এ পরিবর্তন হওয়ার সময় কতটি ইলেকট্রন গ্রহণ হয়, এটি জানাতে বলা হয়েছে। অপশন বিশ্লেষণ: A. একটি ইলেকট্রন গ্রহণ করে: ভুল, এটি সঠিক নয়। B. সাতটি ইলেকট্রন গ্রহণ করে: ভুল, এটি সঠিক নয়। C. পাঁচটি ইলেকট্রন গ্রহণ করে: সঠিক, এটি সঠিক উত্তর। D. তিনটি ইলেকট্রন গ্রহণ করে: ভুল, এটি সঠিক নয়। নোট: KMnO4 থেকে Mn2+ এ পরিবর্তন হওয়ার সময় পাঁচটি ইলেকট্রন গ্রহণ করা হয়।
47
[Fe(CN)6]-3 আয়নে Fe এর জারণ সংখ্যা কত?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: আয়নের জারণ সংখ্যা নির্ণয় করতে হবে। Fe(CN)6]-3 আয়নের জন্য Fe এর জারণ সংখ্যা নির্ধারণের জন্য সমীকরণ ব্যবহার করা যায়। অপশন বিশ্লেষণ: A. -3: ভুল, এটি সঠিক নয়। B. -6: ভুল, এটি অত্যন্ত কম। C. 3: সঠিক, Fe এর জারণ সংখ্যা এখানে +3। D. -2: ভুল, এটি সঠিক মান নয়। নোট: জারণ সংখ্যা নির্ণয়ে আয়ন ও লিগ্যান্ডের মোট চার্জের হিসাব গুরুত্বপূর্ণ।
48
NTP-তে \( \text{H}_2\text{SO}_4 \)-এর জলীয় দ্রবণে কী পরিমাণ তড়িৎ চালনা করলে ক্যাথোডে 5 মোল হাইড্রোজেন গ্যাস বিমুক্ত হয়?
correct
ব্যাখ্যা:
প্রশ্ন বিশ্লেষণ: NTP তে \( \text{H}_2\text{SO}_4 \)-এর জলীয় দ্রবণে ক্যাথোডে 5 মোল হাইড্রোজেন উৎপন্ন করার জন্য কত তড়িৎ প্রয়োজন তা নির্ধারণ করতে বলা হয়েছে। ফারাডের সূত্র অনুসারে, এক মোল গ্যাস উৎপন্ন করতে 2 ফারাড তড়িৎ প্রয়োজন। অপশন বিশ্লেষণ: A. 10 F: সঠিক, \( 5 \times 2 = 10 \)। B. 1 F: ভুল, এটি অত্যন্ত কম। C. 0.1 F: ভুল, এটি অত্যন্ত কম। D. কোনটিই নয়: ভুল, সঠিক উত্তর রয়েছে। নোট: ফারাডের সূত্র ব্যবহার করে এই প্রশ্নের উত্তর নির্ণয় করা হয়।
49
\( \left| \begin{matrix} 2 & -1 & 5 \\ 4 & 3 & -2 \\ 1 & 0 & 6 \end{matrix} \right| \) নির্ণায়কটির \0\" এর সহগুণক কোনটি?"
correct
53
x+y = 4 রেখাটি অক্ষদ্বয়ের সাথে যে ক্ষেত্র তৈরী করে তার ক্ষেত্রফল কত বর্গ একক?
correct
56
একটি ত্রিভুজের কোণগুলোর অনুপাত 2 : 3 : 7 হলে ক্ষুদ্রতম কোণের পরিমাণ কত ডিগ্রী?
skipped
61
\( \left| \begin{matrix} 1 & \omega & \omega^2 \\ \omega & \omega^2 & 1 \\ \omega^2 & 1 & \omega \end{matrix} \right| \) এর মান কোনটি?
correct
64
\( x^2 - 4x + 3 = 0 \) সমীকরণের মূলদ্বয় \( \alpha \) ও \( \beta \) হলে, \( \alpha - \beta \) =?
incorrect
65
\( 4x^2+25y^2 =100 \) উপবৃত্ত দ্বারা আবদ্ধ ক্ষেত্রের ক্ষেত্রফল কত বর্গ একক?
correct
67
\( y^2 = 4px \) পরাবৃত্তটির (3,-2) বিন্দু দিয়ে গমন করলে উপকেন্দ্রিক লম্বের দৈর্ঘ্য কত একক?
correct
70
একটি বিন্দুতে 1,2 ও \( \sqrt{3} \) একক বলত্রয় ক্রিয়া করে সাম্যাবস্থা সৃষ্টি করে। শেষ দুটি বলের মধ্যবর্তী কোণ কোনটি?
correct
71
সমমানের দুইটি বলের লব্ধির বর্গ বলদ্বয়ের গুণফল এর তিনগুণ। এদের মধ্যবর্তী কোণ কত?
incorrect
72
ভূমি হতে \( v \) বেগে খাড়া উপরের দিক নিক্ষিপ্ত বস্তুর সর্বাধিক উচ্চতা কোনটি?
correct
75
10g ভর এর একটি বুলেট 3kg ভরের একটি বন্দুক থেকে 300m/s বেগে বের হলে বন্দুকের পশ্চাৎ বেগ কত?
correct
76
6 একক ভরের একটি কণার অবস্থান (2, 1,4) বিন্দুতে হলে X অক্ষের সাপেক্ষে এর জড়তার ভ্রামক কত হবে?
incorrect
77
1200 kg ভরের একটি গাড়ি 20ms -1 দ্রুতিতে চলছিল। অতঃপর গাড়িটি
800 kg ভরের একটি স্থির গাড়িকে ধাক্কা দিল। ধাক্কার পর গাড়ি দুটি
একত্রিত হয়ে 120 m পিছলায়ে থেমে গেল। বাধাদানকারী বলের মান কত?
skipped
78
প্রশ্ন-৬৯20 kg ভরের একটি পাথর কত উঁচু থেকে পড়লে এর গতিশক্তি 20 ms-1 বেগে চলমান 2000 kg গাড়ির গতিশক্তির সমান হবে?
79
একটি বিদ্যুত কেন্দ্রের সরবরাহকৃত বিদ্যুতশক্তি দ্বারা প্রতি সেকেন্ডে 50 J কাজ করা যায়। বিদ্যুত কেন্দ্রটির ক্ষমতা কত?
correct
80
(৬গ)প্রশ্ন-১৪
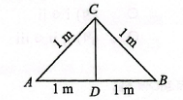 <A ও B বিন্দুতে যথাক্রমে 1 কেজি ও 2 কেজি ভরের বস্তু আছে।< G=6.67x10^-11 Nm^2Kg^-2
<A ও B বিন্দুতে যথাক্রমে 1 কেজি ও 2 কেজি ভরের বস্তু আছে।< G=6.67x10^-11 Nm^2Kg^-2
C ও D বিন্দুতে মহাকর্ষীয় বিভবের অনুপাত কত?