Explanation:
Another Explanation (5): ```html
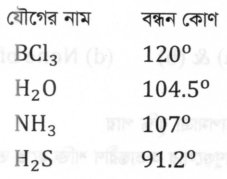
কোন অণুর বন্ধন কোণ সবচেয়ে ছোট? 🤔
প্রদত্ত অণুগুলোর মধ্যে H2S এর বন্ধন কোণের মান সবচেয়ে ছোট। এর কারণগুলো নিচে আলোচনা করা হলো:
বন্ধন কোণ কী? 📐
কোনো অণুতে কেন্দ্রীয় পরমাণুর সাথে যুক্ত অন্যান্য পরমাণুগুলোর মধ্যকার কোণকে বন্ধন কোণ বলে। এটি অণুর আকৃতি এবং ধর্ম নির্ধারণ করে।
কারণসমূহ: H2S-এর বন্ধন কোণ কম হওয়ার কারণ
- কেন্দ্রীয় পরমাণুর তড়িৎ ঋণাত্মকতা: সালফার (S) এর তড়িৎ ঋণাত্মকতা অক্সিজেনের (O) চেয়ে কম। H2O-তে অক্সিজেন পরমাণু বন্ধন ইলেকট্রনগুলোকে নিজের দিকে বেশি টানে, ফলে বন্ধন জোড়গুলোর মধ্যে বিকর্ষণ বেশি হয় এবং বন্ধন কোণ বৃদ্ধি পায়। H2S-এ সালফার কম তড়িৎ ঋণাত্মক হওয়ায় ইলেকট্রনগুলো কম আকৃষ্ট হয়। 🧲
- কেন্দ্রীয় পরমাণুর আকার: সালফারের আকার অক্সিজেনের চেয়ে বড়। আকারের কারণে বন্ধন জোড় ইলেকট্রনগুলো আরও দূরে অবস্থান করে, ফলে বিকর্ষণ কম হয় এবং বন্ধন কোণ ছোট হয়ে যায়। 🐘
- মুক্তজোড় ইলেকট্রন (Lone Pair): অক্সিজেন এবং সালফার উভয়েরই দুটি করে মুক্তজোড় ইলেকট্রন রয়েছে। এই মুক্তজোড় ইলেকট্রনগুলো বন্ধন জোড় ইলেকট্রনগুলোর মধ্যে বিকর্ষণ সৃষ্টি করে। H2O এর তুলনায় H2S এ মুক্তজোড় ইলেকট্রনগুলোর বিকর্ষণ কম, কারণ সালফারের আকার বড় হওয়ায় ইলেকট্রনগুলো কিছুটা ছড়ানো থাকে। 👻
- হাইড্রোজেনের মধ্যে বিকর্ষণ: H2O অণুতে দুটি হাইড্রোজেন পরমাণু অক্সিজেনের কাছাকাছি থাকে বলে এদের মধ্যে সামান্য বিকর্ষণ কাজ করে যা বন্ধন কোণকে কিছুটা বাড়িয়ে দেয়। H2S অণুতে সালফারের আকার বড় হওয়ায় হাইড্রোজেনের মধ্যে বিকর্ষণ তুলনামূলকভাবে কম হয়।
তুলনামূলক আলোচনা: 📊
| অণু |
বন্ধন কোণ (প্রায়) |
| H2O |
104.5° |
| H2S |
92° |
| NH3 |
107° |
| CH4 |
109.5° |
উপরের টেবিল থেকে স্পষ্ট যে H2S এর বন্ধন কোণ অন্যান্য অণুগুলোর তুলনায় উল্লেখযোগ্যভাবে কম।
সারসংক্ষেপ: ✅
H2S অণুতে সালফারের কম তড়িৎ ঋণাত্মকতা, বড় আকার এবং মুক্তজোড় ইলেকট্রনের কারণে বন্ধন কোণ সবচেয়ে ছোট হয়।
আশা করি, ব্যাখ্যাটি বোধগম্য হয়েছে। 😊
```

