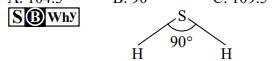Explanation:
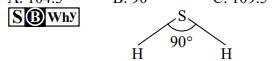
Another Explanation (5): ```html
H2S অণুর বন্ধন কোণ: ৯০°🤔
H2S (হাইড্রোজেন সালফাইড) একটি V-আকৃতির অণু। এর কেন্দ্রীয় পরমাণু সালফার (S)।
বন্ধন কোণ ≈ ৯০° হওয়ার কারণ:
- সালফারের যোজ্যতা স্তরের ইলেকট্রন: সালফারের যোজ্যতা স্তরে ৬টি ইলেকট্রন আছে। এর ইলেকট্রন বিন্যাস: 1s2 2s2 2p6 3s2 3p4। এখানে দুটি বিজোড় ইলেকট্রন (3p4) দুটি হাইড্রোজেনের সাথে সমযোজী বন্ধন গঠন করে।
- VSEPR তত্ত্বানুসারে: VSEPR (Valence Shell Electron Pair Repulsion) তত্ত্ব অনুযায়ী, H2S -এ সালফারের চারপাশে চারটি ইলেকট্রন জোড় আছে: দুটি বন্ধন জোড় (bonding pair) এবং দুটি নিঃসঙ্গ জোড় (lone pair)।
- আদর্শ চতুস্তলীয় কোণ নয় কেন? নিঃসঙ্গ জোড়গুলোর বিকর্ষণ বন্ধন জোড়গুলোর চেয়ে বেশি হওয়ায় বন্ধন কোণ স্বাভাবিক চতুস্তলীয় কোণ (109.5°) থেকে কMe কম হয়। অক্সিজেনের চেয়ে সালফারের আকার বড় হওয়ায় নিঃসঙ্গ ইলেকট্রন জোড়গুলোর বিকর্ষণ তুলনামূলকভাবে কম হয়। ফলে বন্ধন কোণ 92° এর কাছাকাছি থাকে।📚
- p-অরবিটালের প্রভাব: H2S এর বন্ধন মূলত p-অরবিটালের মাধ্যমে গঠিত হয়। বিশুদ্ধ p-অরবিটালের মধ্যে বন্ধন কোণ ৯০° হওয়ার কথা। এখানে s-অরবিটালের সামান্য মিশ্রণ থাকায় বন্ধন কোণ সামান্য বৃদ্ধি পায়।
নোট: পরীক্ষাগারে H2S এর বন্ধন কোণ измерен составляет 92.1°। তবে তাত্ত্বিকভাবে এর মান ৯০° ধরা হয়।🧪
সুতরাং, H2S অণুতে H-S-H বন্ধন কোণের মান প্রায় ৯০°।🧮
```