
নিম্নের যৌগগুলির কোনটির বন্ধন কোণ সবচেয়ে বেশি?
A.
H2O
B.
PCl3
C.
H2S
D.
PH3
নিম্নের যৌগগুলির কোনটির বন্ধন কোণ সবচেয়ে বেশি?
সঠিক উত্তরঃ B.
PCl3
Explanation:
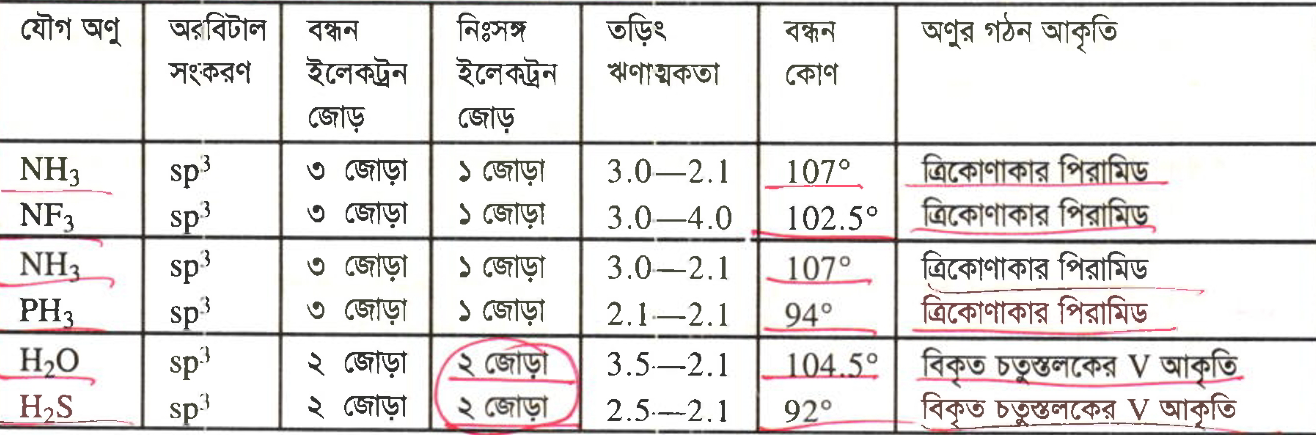
Another Explanation (5):
PCl3 এর বন্ধন কোণ অন্যান্য যৌগগুলোর মধ্যে বেশি হওয়ার কারণ মূলত এর গঠন এবং lone pair ইলেকট্রনের প্রভাব। নিচে বিস্তারিত আলোচনা করা হলো:
| যৌগ | বন্ধন কোণ (প্রায়) | Lone Pair |
|---|---|---|
| PCl3 | 100° | 1 ☝️ |
| NH3 | 107° | 1 ☝️ |
| H2O | 104.5° | 2 ✌️ |
ব্যাখ্যা: PCl3 যৌগে ফসফরাসের তড়িৎ ঋণাত্মকতা ক্লোরিনের তুলনায় কম হওয়ায় এবং lone pair ইলেকট্রনের বিকর্ষণ সত্ত্বেও এর বন্ধন কোণ NH3 এবং H2O এর চেয়ে বেশি। অ্যামোনিয়া (NH3) এবং পানির (H2O) lone pair ইলেকট্রন PCl3 এর চেয়ে বেশি বিকর্ষণ করে তাই এদের বন্ধন কোণ তুলনামূলকভাবে কম। 😥
সুতরাং, lone pair ইলেকট্রনের উপস্থিতি এবং কেন্দ্রীয় পরমাণুর তড়িৎ ঋণাত্মকতার পার্থক্যের কারণে PCl3 এর বন্ধন কোণ প্রদত্ত যৌগগুলোর মধ্যে সবচেয়ে বেশি। 🎉
আশা করি, বুঝতে পেরেছেন! 👍