Explanation:
Another Explanation (5):
AlCl3 যৌগের বৈশিষ্ট্য বিশ্লেষণ 🧪
অ্যালুমিনিয়াম ক্লোরাইড (AlCl3) একটি গুরুত্বপূর্ণ রাসায়নিক যৌগ। এর বৈশিষ্ট্যগুলো হলো:
আলোচনা:
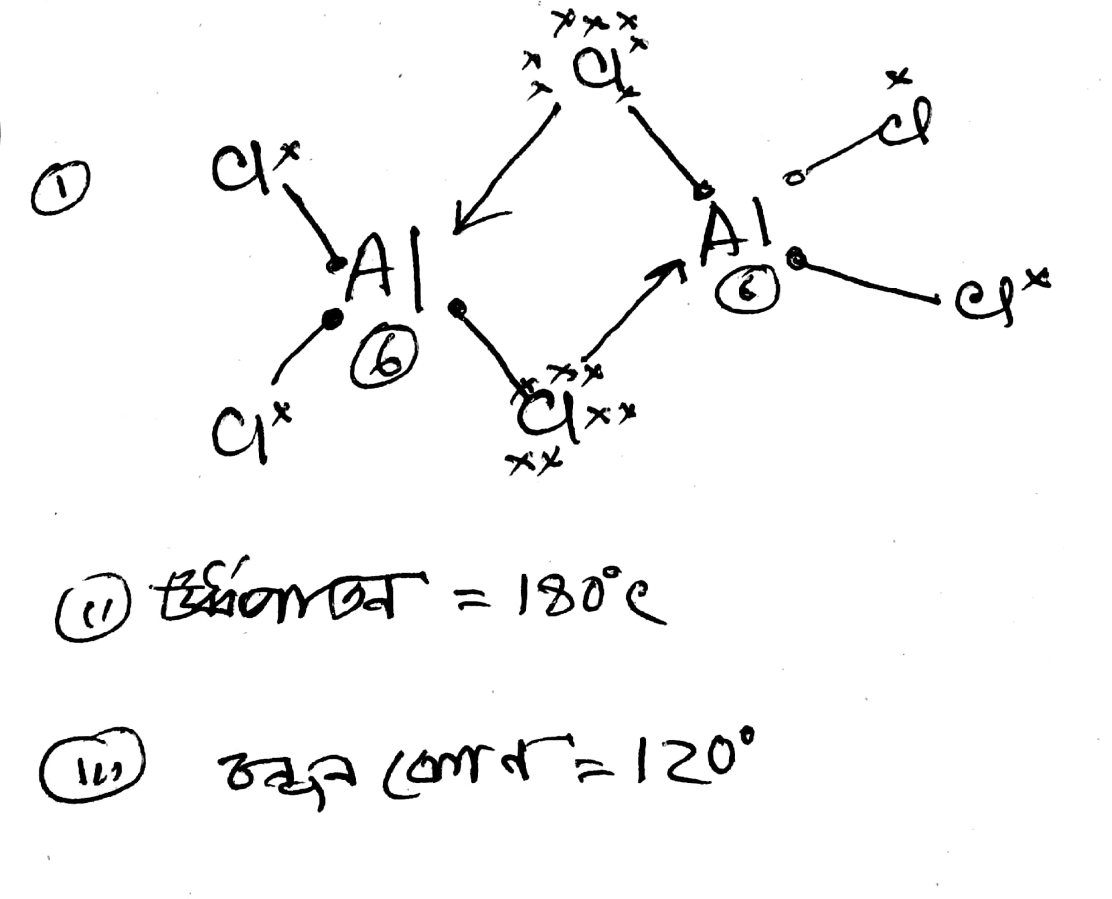
- ডাইমারে 16 জোড়া মুক্ত ইলেকট্রন আছে: AlCl3 গ্যাসীয় অবস্থায় ডাইমার (Al2Cl6) গঠন করে। প্রতিটি ক্লোরিন পরমাণুর তিনটি নিঃসঙ্গ ইলেকট্রন জোড় আছে। Al2Cl6 -এ ৬টি ক্লোরিন পরমাণু থাকায়, মোট নিঃসঙ্গ ইলেকট্রন জোড় এর সংখ্যা = ৬ x ৩ = ১৮। সুতরাং, AlCl3 ডাইমারের কাঠামোতে ১৮ জোড়া নিঃসঙ্গ ইলেকট্রন বিদ্যমান। তাই প্রথম উক্তিটি ভুল।❌
- ঊর্ধ্বপাতন তাপমাত্রা 180°C: AlCl3 এর ঊর্ধ্বপাতন তাপমাত্রা প্রায় 180°C। এই তাপমাত্রায় কঠিন AlCl3 সরাসরি গ্যাসীয় অবস্থায় রূপান্তরিত হয়। অর্থাৎ, এটি তরল অবস্থায় যায় না। ✅
- বন্ধন কোণ 120°: গ্যাসীয় অবস্থায় AlCl3 sp2 সংকরিত এবং ত্রিকোণীয় প্ল্যানার জ্যামিতিযুক্ত। Al-Cl বন্ধনগুলির মধ্যেকার কোণ 120°। কঠিন অবস্থায় AlCl3 ডাইমার গঠন করে এবং চতুস্তলকীয় জ্যামিতি লাভ করে। ✅
Al2Cl6 ডাইমারের গঠন:
| বৈশিষ্ট্য |
মান |
| মোট নিঃসঙ্গ ইলেকট্রন জোড় |
১৮ জোড়া |
| Al-Cl বন্ধন সংখ্যা |
৬টি প্রান্তীয় এবং ২টি সেতু বন্ধন |
সারসংক্ষেপ:
উপরের আলোচনা থেকে এটি স্পষ্ট যে:
- ডাইমারে ১৮ জোড়া মুক্ত ইলেকট্রন আছে।
- AlCl3 এর ঊর্ধ্বপাতন তাপমাত্রা 180°C।
- গ্যাসীয় অবস্থায় AlCl3 এর বন্ধন কোণ 120°।
সুতরাং, সঠিক উত্তর হলো: ii, iii 🎉
আশা করি, এই ব্যাখ্যাটি AlCl3 যৌগটির বৈশিষ্ট্য সম্পর্কে আপনার ধারণা স্পষ্ট করতে সহায়ক হবে।😊

