
A. CH4
B. NH3
C. CO2
D. H2O
সঠিক উত্তরঃ D. H2O
Explanation:
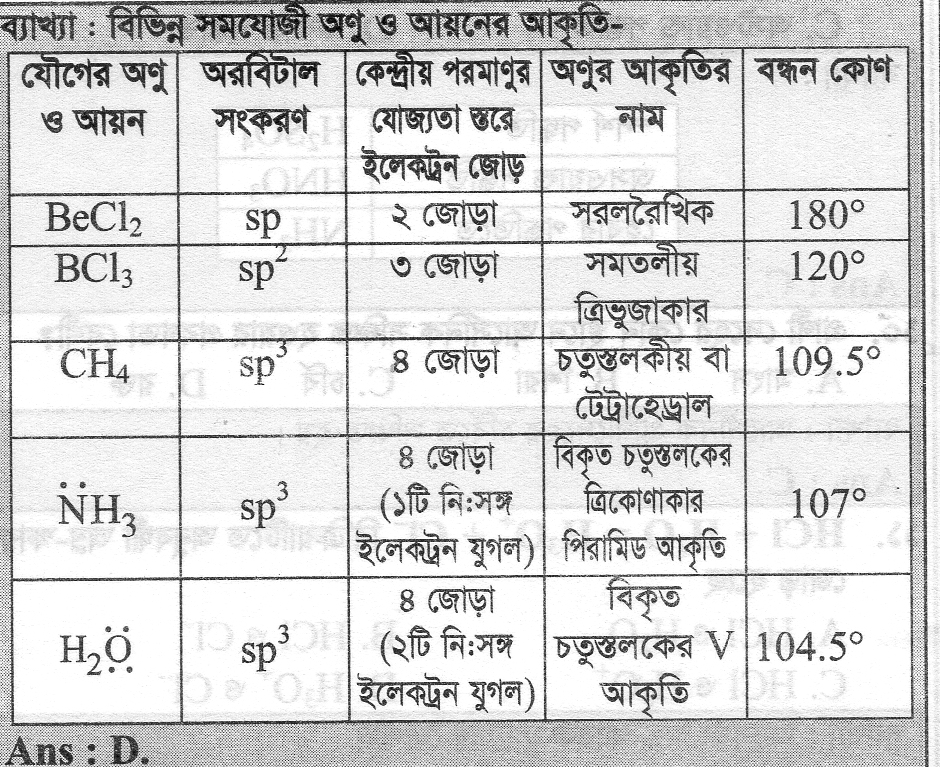
Another Explanation (5):
H2O যৌগের বন্ধনকোণ অন্যান্য যৌগগুলোর তুলনায় ছোট হওয়ার কারণ মূলত এর কেন্দ্রীয় পরমাণু অক্সিজেনের নিঃসঙ্গ ইলেকট্রন জোড় (lone pair) এবং এর গঠন। নিচে বিস্তারিত আলোচনা করা হলো:
কোনো অণুর কেন্দ্রীয় পরমাণুর সাথে যুক্ত দুটি বন্ধন যে কোণ তৈরি করে, তাকে বন্ধনকোণ বলে। বন্ধনকোণ অণুর আকৃতি এবং ধর্ম নির্ধারণে গুরুত্বপূর্ণ ভূমিকা পালন করে।
👇 নিচে একটি টেবিলের সাহায্যে বিষয়টি আরও স্পষ্ট করা হলো:
| বৈশিষ্ট্য | H2O |
|---|---|
| কেন্দ্রীয় পরমাণু | অক্সিজেন (O) |
| বন্ধন জোড় | ২ |
| নিঃসঙ্গ ইলেকট্রন জোড় | ২ |
| প্রত্যাশিত আকৃতি | চতুস্তলকীয় (কিন্তু নিঃসঙ্গ জোড়ের প্রভাবে কৌণিক) |
| আসল আকৃতি | কৌণিক (Bent) 📐 |
| বন্ধনকোণ | ১০৪.৫° |
অক্সিজেনের নিঃসঙ্গ ইলেকট্রন জোড়গুলো বন্ধন জোড়গুলোর চেয়ে বেশি স্থান দখল করে। এর ফলে তারা বন্ধন জোড়গুলোকে আরও কাছে ঠেলে দেয়। নিঃসঙ্গ ইলেকট্রন জোড়ের प्रतिकর্ষণের ক্রম হলো:
নিঃসঙ্গ জোড় - নিঃসঙ্গ জোড় > নিঃসঙ্গ জোড় - বন্ধন জোড় > বন্ধন জোড় - বন্ধন জোড়
এ কারণে H2O এর বন্ধনকোণ ১০৯.৫° (চতুস্তলকীয় কোণ) থেকে কমে ১০৪.৫° হয়।
NH3 (অ্যামোনিয়া)-এর একটি নিঃসঙ্গ ইলেকট্রন জোড় থাকায় এর বন্ধনকোণ ১০৭° (যা H2O থেকে বেশি)। CH4 (মিথেন)-এ কোনো নিঃসঙ্গ ইলেকট্রন জোড় না থাকায় এর বন্ধনকোণ ১০৯.৫°।
H2O যৌগের বন্ধনকোণ সবচেয়ে ছোট হওয়ার মূল কারণ হলো অক্সিজেনের দুটি নিঃসঙ্গ ইলেকট্রন জোড়ের উপস্থিতি, যা বন্ধন জোড়গুলোর মধ্যে বেশি বিকর্ষণ তৈরি করে এবং বন্ধনকোণকে সংকুচিত করে।
আশা করি, ব্যাখ্যাটি বোধগম্য হয়েছে! 👍