
A. CH4
B. H2O
C. BF3
D. CCl4
সঠিক উত্তরঃ C. BF3
Explanation:
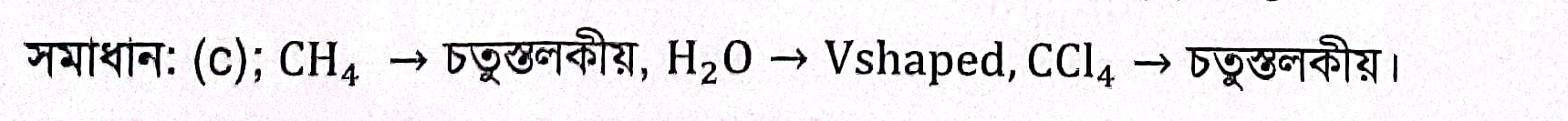
Another Explanation (5):
BF3 (বোরন ট্রাইফ্লুরাইড) একটি ত্রিভুজাকৃতির অণু। এর কারণ হল কেন্দ্রীয় বোরন পরমাণুর চারপাশে তিনটি ফ্লোরিন পরমাণু সমভাবে বিন্যস্ত থাকে। নিচে বিস্তারিত আলোচনা করা হলো:
VSEPR (Valence Shell Electron Pair Repulsion) তত্ত্ব অনুসারে, অণুর গঠন এমনভাবে হয় যাতে ইলেকট্রন জোড়গুলোর মধ্যে বিকর্ষণ সর্বনিম্ন হয়। BF3 এর ক্ষেত্রে, বোরন পরমাণুর চারপাশে তিনটি বন্ধন জোড় (bond pair) ইলেকট্রন থাকে এবং কোনো নিঃসঙ্গ জোড় (lone pair) ইলেকট্রন থাকে না।
VSEPR তত্ত্ব অনুযায়ী, তিনটি বন্ধন জোড় ইলেকট্রন থাকলে তারা একে অপরের থেকে যতটা সম্ভব দূরে থাকতে চায়। এই কারণে তারা ত্রিকোণীয় প্ল্যানার (trigonal planar) গঠন তৈরি করে, যেখানে বন্ধন কোণগুলো ১২০° হয়।
| বৈশিষ্ট্য | BF3 |
|---|---|
| আকৃতি | ত্রিকোণীয় প্ল্যানার (Trigonal Planar) |
| বন্ধন কোণ | ১২০° |
| মেরুতা | অ-মেরু (Non-polar) - কারণ প্রতিটি বন্ধনের ডাইপোল মোমেন্ট একে অপরকে প্রশমিত করে। |
| অণুর উদাহরণ | BCl3, AlCl3 |
BF3 অণুর ত্রিমাত্রিক গঠন অনেকটা নিচের চিত্রের মতো:

সংক্ষেপে, BF3 অণুর ত্রিভুজাকৃতির হওয়ার মূল কারণ হল বোরন পরমাণুর চারপাশে তিনটি ফ্লোরিন পরমাণুর সমভাবে বিন্যস্ত থাকা এবং VSEPR তত্ত্বের প্রভাবে ইলেকট্রন জোড়গুলোর মধ্যে সর্বনিম্ন বিকর্ষণ নিশ্চিত করা। 👍
আশা করি, এই ব্যাখ্যা BF3 অণুর গঠন বুঝতে সাহায্য করবে। 😊
কোনো প্রশ্ন থাকলে জিজ্ঞাসা করতে পারেন। ❓