Explanation:
Another Explanation (5): ```html
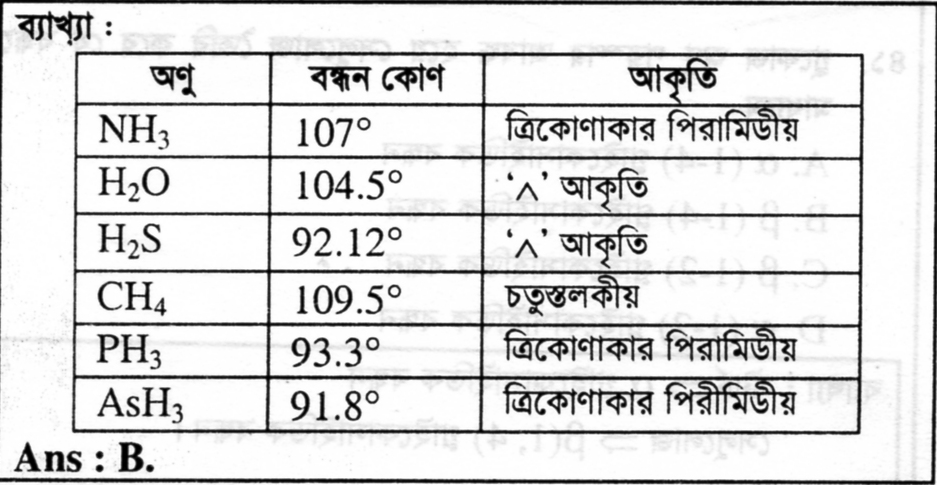
বন্ধন কোণ হ্রাসের সঠিক ক্রম:
\(CH_4 > NH_3 > H_2O > H_2S\)
ব্যাখ্যা:
- \(CH_4\) (মিথেন): এর চতুস্তলীয় জ্যামিতি বিদ্যমান tetrahedral geometry 📐, যেখানে বন্ধন কোণ \(109.5^\circ\)। এখানে কোনো নিঃসঙ্গ ইলেকট্রন জোড় (lone pair of electrons)নেই।
- \(NH_3\) (অ্যামোনিয়া): এর একটি নিঃসঙ্গ ইলেকট্রন জোড় lone pair আছে। নিঃসঙ্গ ইলেকট্রন জোড় lone pair এবং বন্ধন জোড়ের মধ্যে বিকর্ষণের কারণে বন্ধন কোণ \(107^\circ\) এ নেমে আসে। lone pair>bond pair repulsion 😠
- \(H_2O\) (পানি): এতে দুটি নিঃসঙ্গ ইলেকট্রন জোড় আছে। নিঃসঙ্গ ইলেকট্রন জোড়ের increased বিকর্ষণের lone pair repulsion ফলে বন্ধন কোণ আরও কমে \(104.5^\circ\) হয়। lone pair>lone pair repulsion 😡😡
- \(H_2S\) (হাইড্রোজেন সালফাইড): \(H_2O\) এর মতো গঠন হলেও সালফারের তড়িৎ ঋণাত্মকতা অক্সিজেনের চেয়ে কম। ফলে বন্ধন ইলেকট্রন জোড় সালফার নিউক্লিয়াসের থেকে দূরে থাকে এবং নিঃসঙ্গ ইলেকট্রন জোড়ের বিকর্ষণ কম হয়। তাই বন্ধন কোণ \(92^\circ\) এর কাছাকাছি থাকে। S এর আকার বড় হওয়ায় বিকর্ষণ কম হয়। 😊
সারসংক্ষেপ: নিঃসঙ্গ ইলেকট্রন জোড়ের সংখ্যা বৃদ্ধি এবং কেন্দ্রীয় পরমাণুর তড়িৎ ঋণাত্মকতা হ্রাসের সাথে সাথে বন্ধন কোণ হ্রাস পায়। 👍
```

