Explanation:
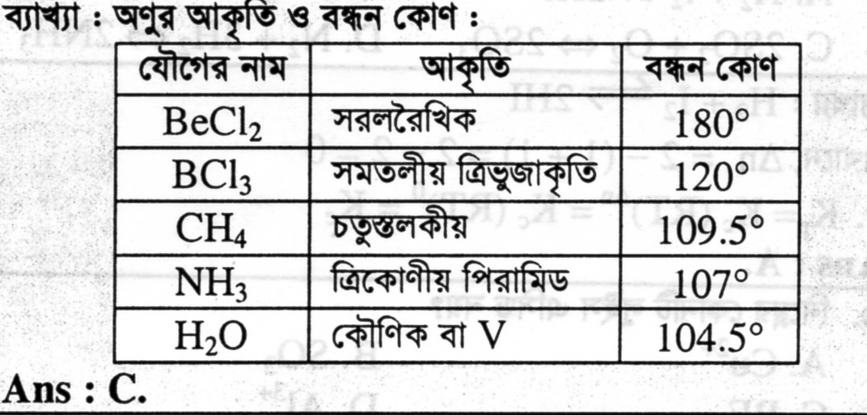
Another Explanation (5):
CH4, NH3, H2O এর বন্ধন কোণের ক্রম ব্যাখ্যা
বন্ধন কোণের ক্রম CH4 > NH3 > H2O হওয়ার কারণ নিচে আলোচনা করা হলো:
মূল ধারণা
- VSEPR তত্ত্ব: বন্ধন কোণ মূলত VSEPR (Valence Shell Electron Pair Repulsion) তত্ত্বের উপর নির্ভর করে। এই তত্ত্ব অনুযায়ী, কোনো পরমাণুর যোজ্যতা স্তরের ইলেকট্রন জোড়গুলো (বন্ধন জোড় ও নিঃসঙ্গ জোড়) নিজেদের মধ্যে বিকর্ষণ করে এবং যতটা সম্ভব দূরে থাকতে চায়।
- নিঃসঙ্গ জোড় (Lone pair): নিঃসঙ্গ জোড় বন্ধন জোড়ের চেয়ে বেশি বিকর্ষণ করে।
আণবিক গঠন এবং বন্ধন কোণ
| আণু |
কেন্দ্রীয় পরমাণু |
বন্ধন জোড় |
নিঃসঙ্গ জোড় |
আকৃতি |
বন্ধন কোণ (প্রায়) |
| CH4 (মিথেন) |
C (কার্বন) |
4 |
0 |
টেট্রাহেড্রাল (চতুস্তলকীয়) tetrahedral |
109.5° 😊 |
| NH3 (অ্যামোনিয়া) |
N (নাইট্রোজেন) |
3 |
1 |
ত্রিকোণাকার পিরামিডীয় (Trigonal pyramidal) ⛰️ |
107° 😥 |
| H2O (পানি) |
O (অক্সিজেন) |
2 |
2 |
বাঁকানো (Bent) 🤸 |
104.5° 😭 |
কারণসমূহ
- মিথেন (CH4): কার্বনের চারটি বন্ধন জোড় আছে এবং কোনো নিঃসঙ্গ জোড় নেই। ফলে এরা সুষমভাবে চতুস্তলকীয় আকারে থাকে এবং বন্ধন কোণ হয় 109.5°।
- অ্যামোনিয়া (NH3): নাইট্রোজেনের তিনটি বন্ধন জোড় এবং একটি নিঃসঙ্গ জোড় আছে। নিঃসঙ্গ জোড় বন্ধন জোড়গুলোর উপর বিকর্ষণ বল প্রয়োগ করে, ফলে বন্ধন কোণ সামান্য কমে 107° হয়।
- পানি (H2O): অক্সিজেনের দুটি বন্ধন জোড় এবং দুটি নিঃসঙ্গ জোড় আছে। এখানে নিঃসঙ্গ জোড়ের বিকর্ষণ আরও বেশি হওয়ার কারণে বন্ধন কোণ আরও কমে 104.5° হয়।
সংক্ষেপে
নিঃসঙ্গ জোড়ের সংখ্যা বৃদ্ধির সাথে সাথে বন্ধন কোণ কমতে থাকে। 📉
- CH4: কোনো নিঃসঙ্গ জোড় নেই ➡️ বন্ধন কোণ সর্বোচ্চ
- NH3: একটি নিঃসঙ্গ জোড় ➡️ বন্ধন কোণ মাঝারি
- H2O: দুটি নিঃসঙ্গ জোড় ➡️ বন্ধন কোণ সর্বনিম্ন
অতএব, বন্ধন কোণের ক্রম: CH4 > NH3 > H2O। 🎉

